Системные глюкокортикоиды при бронхиальной астме. Лечение
Глюкокортикостероиды (ГК) широко применяются практически во всех отраслях медицины, в том числе и в пульмонологии. Они являются базисными, т.е. основными, в лечении всех патогенетических вариантов бронхиальной астмы персистирующего течения, начиная с легкой степени тяжести. Тем не менее, как показывает опыт, назначение ГК вызывает опасения не только у пациентов, но даже у врачей. Несвоевременная и неадекватная стероидная терапия может привести не только к неконтролируемому течению бронхиальной астмы, но и к развитию жизнеугрожающих состояний, требующих назначения гораздо более серьезной системной стероидной терапии. В свою очередь длительная системная стероидная терапия даже небольшими дозами может сформировать ятрогенные болезни и синдромы (васкулит, остеопороз, синдром Иценко–Кушинга, ожирение, артериальную гипертензию, сахарный диабет, миодистрофию и т.д.). Мы попытаемся ответить на вопрос, как можно контролировать бронхиальную астму безопасными и эффективными стероидами и как избежать возможных осложнений.
Итак, целями лечения больных бронхиальной астмой являются:
Достижение и поддержание контроля над симптомами.
Предотвращение обострений.
Поддержание показателей функции внешнего дыхания, максимально приближенных к нормальному уровню.
Отсутствие ограничений физической активности, включая занятия физкультурой и спортом.
Отсутствие побочных эффектов и нежелательных явлений от лекарственных препаратов.
Предотвращение формирования необратимой бронхиальной обструкции.
Предотвращение смертности от астмы.
Эти цели отражают понимание бронхиальной астмы, как хронического заболевания с прогрессирующим развитием воспалительного процесса в дыхательных путях, ведущего к проявлению различных симптомов болезни (от незначительных до ярко выраженных) в зависимости от степени этого воспаления. В связи с этим целесообразно напомнить читателям современное определение бронхиальной астмы, приведенное в "Глобальной стратегии лечения и профилактики бронхиальной астмы"; (GINA-2002):
Бронхиальная астма – хроническое воспалительное заболевание дыхательных путей, в котором играют роль многие клетки и клеточные элементы. Хроническое воспаление вызывает сопутствующее повышение гиперреактивности дыхательных путей, приводящее к повторяющимся эпизодам свистящих хрипов, одышки, чувства стеснения в груди и кашля, особенно ночью или ранним утром. Эти эпизоды обычно связаны с распространенной, но изменяющейся по своей выраженности бронхиальной обструкцией, которая часто является обратимой либо спонтанно, либо под влиянием лечения.
В настоящее время бронхиальную астму следует классифицировать в первую очередь по степени тяжести, так как именно это отражает степень выраженности воспалительного процесса в дыхательных путях и определяет тактику противовоспалительной терапии.
Степень тяжести
определяется по следующим показателям:
1. Количество ночных симптомов в неделю.
2. Количество дневных симптомов в день и в неделю.
3. Кратность применения beta2-агонистов короткого действия.
4. Выраженность нарушений физической активности и сна.
5. Значения пиковой скорости выдоха (ПСВ) и ее процентное соотношение с должным или наилучшим значением.
6. Суточные колебания ПСВ.
7. Объем проводимой терапии.
Наиболее важными, как нам кажется, в определении степени тяжести являются не только и не столько симптомы и показатели функции внешнего дыхания (ФВД), сколько объем базисной терапии, необходимый для поддержания нормальной жизнедеятельности человека.
Ступенчатый подход
к терапии бронхиальной астмы отражает объем проводимой терапии в зависимости от тяжести ее течения. Как видно из представленных таблиц, все препараты для лечения бронхиальной астмы разделены на две основные группы: для длительного контроля воспалительного процесса (основные и альтернативные) и для купирования острых симптомов астмы. Основой терапии для длительного контроля воспалительного процесса являются ингаляционные глюкокортикоиды (ИГКС), которые следует применять при персистирующей бронхиальной астме любой степени тяжести. В настоящее время ИГКС рассматриваются в качестве средств первой линии в терапии бронхиальной астмы.
Чем выше степень тяжести течения бронхиальной астмы, тем большие дозы ингаляционных стероидов следует применять. По данным ряда исследований, у пациентов, начавших лечение ИГКС не позже 2 лет от начала заболевания, отмечены существенные преимущества в улучшении контроля над симптомами астмы, по сравнению с начавшими такую терапию по прошествии 5 лет и более.
Противовоспалительный эффект ИГКС связан с их ингибирующим действием на клетки воспаления и их медиаторы, включая продукцию цитокинов, вмешательство в метаболизм арахидоновой кислоты и синтез лейкотриенов и простагландинов, снижение проницаемости микрососудов, предотвращение прямой миграции и активации клеток воспаления, повышение чувствительности beta-рецепторов гладкой мускулатуры. ИГКС увеличивают синтез противовоспалительных белков (липокортина-1), увеличивают апоптоз и снижают количество эозинофилов путем ингибирования интерлейкина-5. Таким образом, ИГКС приводят к стабилизации клеточных мембран, уменьшают проницаемость сосудов, улучшают функцию beta-рецепторов как путем синтеза новых, так и повышая их чувствительность, стимулируют эпителиальные клетки.
ИГКС отличаются от системных глюкокортикостероидов своими фармакологическими свойствами: липофильностью, быстротой инактивации, коротким периодом полувыведения из плазмы крови. Важно учитывать, что лечение ИГКС является местным (топическим), что обеспечивает выраженные противовоспалительные эффекты непосредственно в бронхиальном дереве при минимальных системных проявлениях. Количество ИГКС, доставляемое в дыхательные пути, зависит от номинальной дозы препарата, типа ингалятора, наличия или отсутствия пропеллента, а также техники выполнения ингаляции. Следует учитывать, что около 80% пациентов испытывают сложности при использовании дозированных аэрозолей.
Наиболее важной характеристикой для проявления селективности и времени задержки препарата в тканях является липофильность. Благодаря липофильности ИГКС накапливаются в дыхательных путях, замедляется их высвобождение из тканей и увеличивается их сродство к глюкокортикоидному рецептору. Высоколипофильные ИГКС быстрее и лучше захватываются из просвета бронхов и длительно задерживаются в тканях дыхательных путей. Наиболее высокой липофильностью и противовоспалительной активностью обладает флутиказон пропионат (фликсотид), что позволяет применять его в меньших дозах. Будесонид (пульмикорт), как показали исследования, образует внутриклеточные конъюгаты, также обладающие выраженной липофильностью. Именно липофильность ИГКС отличает их от системных препаратов, поэтому бесполезно назначать ингаляции системных ГКС (гидрокортизона, преднизолона и дексаметазона) – эти препараты вне зависимости от способа применения обладают только системным действием.
К ИГКС относятся беклометазон дипропионат (БДП), будесонид (БУД), флутиказон пропионат (ФП), флунизолид (ФЛУ) и триамцинолона ацетонид (ТА), мометазона фуроат. Они выпускаются в виде дозированных аэрозолей, сухой пудры, а также в виде растворов для использования в небулайзерах.
В многочисленных рандомизированных плацебо-контролируемых исследованиях у больных бронхиальной астмой показана эффективность всех доз ИГКС в сравнении с плацебо (уровень доказательности А). Все ИГКС в эквипотентных дозах обладают противовоспалительным действием (уровень доказательности А). Итак, в GINA-2002 введено понятие эквипотентных, или эквивалентных, доз, указывающее на то, что различные ИГКС отличаются друг от друга по степени противовоспалительного действия. Приблизительные эквипотентные дозы указаны.
Сведения относительно системного эффекта ИГКС весьма разноречивы. Системная биодоступность складывается из пероральной и легочной. Пероральная доступность зависит от абсорбции в желудочно-кишечном тракте и от выраженности эффекта "первого прохождения" через печень, благодаря чему в системный кровоток поступают уже неактивные метаболиты (за исключением беклометазона 17-монопропионата – активного метаболита беклометазона дипропионата). Легочная биодоступность зависит от процента попадания препарата в легкие (что зависит от типа используемого ингалятора), наличия или отсутствия носителя (лучшие показатели имеют ингаляторы, не содержащие фреон) и от абсорбции препарата в дыхательных путях. Так, например, беклометазон дипропионат с фреоновым носителем (CFC, ХФУ или ХФК – хлорфлюорокарбон) используется в дозах, вдвое больших, чем при использовании бесфреонового носителя (HFA или ГФА – гидрофторалкан). Следует отметить, что дозы ИГКС до 1000 мкг/сут обладают минимальным системным действием, несравнимым с использованием любых системных стероидов.
ИГКС отличаются друг от друга не только показателями системной биодоступности, но и рядом других показателей, определяющих их эффективность и безопасность, в том числе и системное действие.
Таким образом, из представленных выше данных видно, что флутиказон пропионат, обладающий высокой тропностью к ГКР, имеет наиболее выраженное противовоспалительное действие и должен использоваться в дозах, вдвое меньших, чем беклометазон дипропионат и будесонид в сравнимых средствах доставки. Флунизолид для достижения сравнимого противовоспалительного эффекта должен использоваться в более высоких дозах, чем беклометазон и будесонид.
Нежелательные эффекты ИГКС
. Особо следует подчеркнуть, что ИГКС обладают минимальными побочными эффектами при правильном подборе и технике ингаляции. Наиболее часто наблюдаются местные нежелательные проявления: кандидоз полости рта и ротоглотки, дисфония, иногда кашель, возникающий вследствие раздражения верхних дыхательных путей. Однако их зачастую можно предотвратить, если пользоваться устройством со спейсером. Полоскание рта водой (с последующим сплевыванием) после ингаляции и использование спейсера может предотвратить развитие кандидоза полости рта и ротоглотки. Все существующие в настоящее время ИГКС всасываются в легких, и, таким образом, неизбежно некоторая их часть попадает в системный кровоток. Риск системных нежелательных эффектов ингаляционных ГКС зависит от дозы и активности ГКС, а также от биодоступности, всасывания в кишечнике, метаболизма при первом прохождении через печень и периода полувыведения той их части, которая всосалась в легких, и, вероятно, в кишечнике. Поэтому системные эффекты будут различны у разных ингаляционных ГКС. Несколько сравнительных исследований продемонстрировали, что будесонид и флутиказон пропионат обладают меньшим системным действием, чем БДП и триамцинолон. Риск системных эффектов также зависит от типа ингалятора: применение спейсеров уменьшает системную биодоступность и риск системных нежелательных действий большинства ГКС. При использовании турбухалер эффективность будесонида возрастает вдвое.
Комбинированная терапия
Хотя ИГКС являются основой терапии бронхиальной астмы, они не всегда позволяют полностью контролировать проявления астмы. В связи с этим возникала необходимость в назначении ингаляционных beta2-агонистов не только по потребности, но и регулярно. Таким образом, возникла необходимость в препаратах нового класса, свободных от недостатков, которые присущи beta2-агонистам короткого действия, и обладающих доказанным длительным протективным и противовоспалительным действием на дыхательные пути. Были созданы и в настоящее время широко применяются beta2-агонисты длительного действия, которые на фармацевтическом рынке представлены двумя препаратами: сальметеролом ксинафоатом и формотеролом фумаратом. В современных руководствах по терапии астмы рекомендовано добавление beta2-агонистов длительного действия при недостаточном контроле бронхиальной астмы монотерапией ингаляционными глюкокортикоидами (начиная со 2-й ступени). В ряде исследований показано, что комбинация (ИГКС+beta2-агонист длительного действия) более эффективна, чем удвоение дозы ингаляционных глюкокортикоидов, и приводит к более значимому улучшению функции легких и лучшему контролю над симптомами астмы. Было отмечено также снижение количества обострений у пациентов, получающих комбинированную терапию, и значимое улучшение качества их жизни. Таким образом, появление комбинированных препаратов, составными компонентами которых являются ингаляционный кортикостероид и beta2-агонист длительного действия, является отражением эволюции взглядов на терапию бронхиальной астмы.
Главным преимуществом комбинированной терапии является повышение эффективности лечения при использовании более низких доз ИГКС. Кроме того, соединение двух препаратов в одном ингаляторе облегчает пациенту выполнение назначений врача и потенциально улучшает комплайнс.
Следует рассматривать данные классы препаратов (ИГКС и beta2-агонисты длительного действия) как синергисты, что обусловлено их комплементарным воздействием на молекулярном и рецепторном уровнях.
ИГКС увеличивают количество beta-рецепторов и повышают их активность. beta-Рецепторы в свою очередь запускают каскад внутриклеточных биохимических реакций, что приводит к активированию глюкокортикоидного рецептора и образованию активного комплекса ГКС + ГКР под действием меньших доз ИГКС, увеличивают транслокацию активного стероидрецепторного комплекса в ядро, где он взаимодействует со специфичной областью гена-мишени (глюкокортикоидчувствительный элемент, ГЧЭ). Это приводит к усилению противовоспалительной активности и вновь к повышению синтеза beta-рецепторов (см. рисунок).
Контролируемые исследования также показали, что введение ИГКС и beta2-агонистов длительного действия в виде комбинированного препарата столь же эффективно, как и раздельное введение каждого из них (уровень доказательности В). Ингаляторы с фиксированными комбинациями препаратов более удобны для пациентов, повышают комплайнс, обеспечивают одновременное введение beta2-агониста и ИГКС. В настоящее время существуют два препарата с фиксированными комбинациями: флутиказон пропионат плюс сальметерол (серетид) и будесонид плюс формотерол (симбикорт).
Серетид мультидиск.
Составными компонентами являются сальметерол ксинафоат и флутиказон пропионат. Обеспечивает высокий контроль над симптомами бронхиальной астмы. Используется только в качестве базисной терапии. Можно назначать, начиная со второй ступени. Препарат представлен в дозировках 50/100 мкг, 50/250 мкг, 50/500 мкг/доза.
Компоненты, входящие в состав серетида, применяются достаточно давно: флутиказон пропионат – с 1993 года, сальметерол ксинафоат – с 1990 года.
Флутиказон пропионат
– один из самых высокоактивных противовоспалительных препаратов на сегодняшний день. Эквивалентные терапевтические (эквипотентные) дозы флутиказон почти в 2 раза меньше, чем у беклометазона дипропионата. Препарат имеет низкую системную биодоступность (~1%), а абсолютная биодоступность составляет 10–30% в зависимости от типа ингалятора. Флутиказон обладает высоким сродством к глюкокортикоидным рецепторам и имеет длительную связь с рецептором. Для предотвращения осиплости голоса и развития кандидоза при приеме флутиказон следует соблюдать те же правила, что и при приеме других ИГКС, т.е. полоскать рот и горло водой после ингаляции. В связи с высоким противовоспалительным действием флутиказон также показан больным с тяжелым течением бронхиальной астмы и зависимостью от системных ГКС. Дозы флутиказон должны подбираться строго индивидуально в зависимости от тяжести течения, ответа на противовоспалительную терапию и индивидуальной чувствительности пациента.
Сальметерол ксинафоат
относится к ингаляционным beta2-агонистам длительного действия с медленным началом действия. Исследования конца 90-х годов показали, что применение beta2-агонистов длительного действия, к которым относятся сальметерол и формотерол, позволяет не только предупредить ночные симптомы и астму физического усилия, но и уменьшить почти вдвое дозу ИГКС, необходимую для достижения адекватного контроля над бронхиальной астмой. Проведенные клинические исследования показали, что beta2-агонисты длительного действия оказывают стабилизирующее влияние на тучные клетки, ингибируют IgE-опосредованное высвобождение ими гистамина, что приводит к уменьшению системной и местной концентрации гистамина. Они также уменьшают проницаемость легочных капилляров, причем в большей степени, чем ИГКС. Важно отметить, что противовоспалительные эффекты beta2-агонистов длительного действия не могут играть определяющей роли у больных бронхиальной астмой, так как снижение чувствительности beta2-адренорецепторов (десенситизация) и "down"-регуляция (уменьшение количества рецепторов) в клетках воспаления возникает быстрее, чем в миоцитах бронхов. Поэтому при систематическом приеме стимуляторов beta2-адренорецепторов толерантность к их противовоспалительным эффектам развивается достаточно быстро. Однако благодаря способности ИГКС увеличивать число и функцию beta2-адренорецепторов, снижая их десенситизацию и "down"-регуляцию, при совместном назначении ИГКС и beta2-агонистов противовоспалительная активность beta2-агонистов длительного действия может проявляться клинически. Сальметерол назначается только в качестве препарата для базисной терапии и не применяется по потребности. Следует использовать только рекомендованные дозы, а для купирования симптомов использовать beta2-агонисты короткого действия. Следует отметить, что сальметерол обладает и рядом неожиданных свойств, в частности вызывает снижение патогенности P.aeruginosa
и протективный эффект в отношении H.influenzae
в культурах эпителия респираторного тракта.
Клинические исследования, проведенные с препаратом "Серетид", доказали его высокую эффективность. Более того, его эффективность при бронхиальной астме была выше, чем у его компонентов, назначаемых по отдельности.
Серетид выпускается в порошковых ингаляторах мультидиск. Данное ингаляционное устройство позволяет не только точно дозировать препарат, но и подсчитывать дозы. В России серетид доступен в следующих дозировках: 50 мкг сальметерола и 100 мкг флутиказон пропионата; 50 мкг сальметерола и 250 мкг флутиказон пропионата.
Следует помнить, что серетид не назначают для купирования симптомов бронхиальной астмы, для этого предпочтительно назначать beta2-агонисты короткого действия.
В нашей стране проведено исследование качестваа жизни больных бронхиальной астмой, принимающих серетид (ИКАР), подтвердившие, что прием серетида улучшает показатели качества жизни пациентов, способствует сотрудничеству пациента с врачом, он более удобен в применении. Изучение предпочтений пациентов также показало преимущество комбинированного препарата.
Симбикорт турбухалер.
Составными компонентами являются будесонид и формотерол фумарат. На российском рынке представлен в дозировке 160/4,5 мкг/доза (дозы препаратов указаны как доза на выходе).
Препарат обладает быстрым началом действия (в течение 1–3 мин) благодаря быстрому действию формотерола. Можно применять однократно, так как доказано 24-часовое действие будесонида. Все это вместе создает возможность гибкого дозирования препарата.
Системные глюкокортикостероиды
Системные стероиды при бронхиальной астме обычно применяются перорально и значительно реже – внутривенно высокими дозами (пульс-терапия) при обострении заболевания.
Предполагаемые механизмы действия такие же, как у ИГКС. Однако системные ГКС могут достигать других клеток-мишеней, чем ингаляционные ГКС, и формировать при длительном приеме системные осложнения.
Следует отличать назначение системных ГКС при признаках обострения бронхиальной астмы и в качестве препаратов для длительного контроля при персистирующей бронхиальной астме. Назначение системных стероидов для длительного контроля астмы сразу определяет больного как тяжелого и требует назначения высоких доз ИГКС и ингаляционных beta2-агонистов длительного действия (табл. 3–5, ступень 4). Недопустимо контролировать бронхиальную астму только системными стероидами. Неназначение ИГКС при этом является грубой врачебной ошибкой, приводящей к развитию тяжелых системных осложнений при недостаточном контроле воспалительного процесса в легких. Осложнения длительного применения системных ГКС известны: остеопороз, артериальная гипертензия, сахарный диабет, подавление функциональной активности гипоталамо-гипофизарно-надпочечниковой системы, катаракта, глаукома, ожирение, истончение кожи с образованием стрий и повышенной капиллярной проницаемостью, мышечная слабость. Если же необходимость в длительном применении системных ГКС все же возникает, несмотря на максимальный объем ингаляционной терапии, то с момента назначения системной стероидной терапии в любой форме пациент должен получать превентивную терапию по поводу остеопороза.
Следует отметить, что терапевтический индекс (соотношение эффект/нежелательный эффект) при длительном лечении бронхиальной астмы ингаляционными ГКС всегда выше, чем при любой длительной пероральной или парентеральной терапии ГКС. Ингаляционные ГКС более эффективны, чем пероральные, принимаемые через день. Если предстоит длительная терапия пероральными ГКС, необходимо обратить внимание на мероприятия, которые уменьшают системные нежелательные эффекты. Для длительного лечения пероральные препараты предпочтительнее парентеральных. Лучше назначать такие пероральные ГКС, как преднизон, преднизолон или метилпреднизолон, поскольку они обладают минимальным минералокортикоидным эффектом, относительно коротким периодом полувыведения и нерезко выраженным действием на поперечнополосатую мускулатуру. Если это возможно, то их следует назначать через день. Длительный прием триамцинолона нежелателен из-за частого развития мышечной дистрофии, похудания, слабости, поражения желудочно-кишечного тракта; препараты триамцинолона категорически противопоказаны беременным женщинам и детям. Дексаметазон при бронхиальной астме не показан для длительного приема в связи с выраженным подавлением функции коры надпочечников, способностью задерживать жидкости и низкой эффективностью в отношении ГКР в легких.
По возможности, при длительной терапии пероральные ГКС следует назначать 1 раз в сутки, утром, ежедневно или через день. Следует еще раз особо подчеркнуть, что выбор системных ГКС для поддерживающей терапии в настоящее время за короткодействующими препаратами. Применение депонированных форм длительного действия в терапии бронхиальной астмы категорически не рекомендуется.
Любой пациент, которому назначены системные ГКС для контроля бронхиальной астмой, в обязательном порядке подлежит тщательному обследованию с целью установления причин, приведших к необходимости данного вида лечения. Наиболее важными факторами являются: врачебные ошибки при терапии бронхиальной астмы (неназначение ИГКС, недооценка степени тяжести бронхиальной астмы на предшествующих этапах, попытка контроля воспаления в период обострения низкими дозами ГКС, что приводит к назначению системных ГКС на длительный срок, применение beta-блокаторов, неправильный подбор системы доставки для ИГКС), низкий комплайнс, продолжающаяся экспозиция аллергенов. В отдельных случаях имеет место неправильный диагноз бронхиальной астмы, где респираторные симптомы являются следствием другой патологии (системные васкулиты, системная склеродермия, дерматомиозит, бронхолегочный аспергиллез, гастроэзофагеальная рефлюксная болезнь, истерия и т.д.). В 5% случаев встречается стероидорезистентность, для которой характерна резистентность стероидных рецепторов к стероидным препаратам. В настоящее время различают две подгруппы: больные с истинной стероидной резистентностью (тип II), не имеющие побочных эффектов при длительном приеме высоких доз системных глюкокортикоидов, и пациенты с приобретенной резистентностью (тип I), имеющие побочные эффекты от приема системных стероидов. В последней подгруппе резистентность скорее всего можно преодолеть повышением дозы глюкокортикоидов и назначением препаратов, имеющих аддитивный эффект.
Необходима разработка диагностических и лечебных программ для пациентов, получающих системную стероидную терапию. Следует провести тщательную дифференциальную диагностику для исключения других заболеваний, имитирующих клиническую картину бронхиальной астмы.
Перед врачом стоит задача контролировать воспалительный процесс при бронхиальной астме наименьшими поддерживающими дозами как системных, так и ингаляционных ИГКС. Внедрение в клиническую практику высоколипофильных ИГКС, в частности флутиказон пропионата, позволяет значительно снизить или даже полностью отменить системные ГКС. К сожалению, в настоящее время не существует фиксированных схем снижения системных ГКС. Поэтому врач должен правильно оценить клиническую картину заболевания, предположить возможные причины стероидозависимости и назначить максимальные дозы высокоэффективных ИГКС, например флутиказон пропионата. Обязательно в качестве контроля за ФВД рекомендовать применение ежедневной пикфлоумстрии и учет приема beta2-агонистов по потребности. Следует снижать системные ГКС постепенно на фоне постоянного приема высоких доз ИГКС. Нам представляется целесообразным снижать системные ГКС медленно, уменьшая дозу не ранее чем каждые 3–4 нед, во избежание развития осложнений. Целесообразно при каждом уменьшении дозы проводить анализ крови. Возможное нарастание СОЭ и эозинофилии может свидетельствовать о проявлении системного заболевания, в том числе васкулита. Желательно также исследовать базальный уровень кортизола, так как после прекращения длительной терапии супрессивными дозами системных ГКС возможно развитие надпочечниковой недостаточности. На фоне снижения системных ГКС нельзя уменьшать поддерживающие дозы ИГКС. После отмены системных стероидов титрование дозы ИГКС должно проводиться с учетом рекомендаций ступенчатого подхода. Представляется целесообразным назначение комбинированной терапии пациентам с тяжелой стероидозависимой бронхиальной астмой.
Бронхиальная астма
Ингаляционные глюкокортикостероиды: влияние средств доставки на эффективность и безопасность терапии бронхиальной астмы
Н.П. Княжеская
Необходимым условием достижения контроля бронхиальной астмы (БА) является использование адекватных доз ингаляционных глюкокортикостероидов (ИГКС). Лечение ИГКС является местным (топическим), что обеспечивает выраженные противовоспалительные эффекты непосредственно в бронхиальном дереве при минимальных системных проявлениях. Количество ИГКС, доставляемых в дыхательные пути, зависит от номинальной дозы препарата, типа ингалятора, наличия или отсутствия пропеллента, а также от техники выполнения ингаляции. Следует учитывать, что примерно 80% пациентов испытывают сложности при использовании ингаляторов. Использование мультидозового ингалятора Изихейлер в связи с простой техникой ингаляции способствует уменьшению числа ошибок и достижению контроля БА.
Ключевые слова: бронхиальная астма, средства доставки, ингаляционные глюкокортикостероиды, порошковые ингаляторы, Изихейлеры, Будесонид Изихейлер.
История вопроса
В 1896 г. У. Ослер лечил больных глицериновыми экстрактами из свежих надпочечников свиней. Однако только в 1929 г. Ф. Хартманом с сотрудниками были проведены первые клинические испытания экстракта из коры надпочечников, доказавшие его очень высокую терапевтическую эффективность при болезни Аддисона. Ф. Хенч, работавший в 1930-е годы в клинике Мэйо (США), обратил внимание на то, что у пациентов с ревматическими заболеваниями течение заболевания улучшается при беременности или при развитии желтухи. У него возникло предположение, что это, возможно, связано с появлением в организме неких стероидных веществ, близких по строению к половым гормонам или к желчным кислотам, которые выделяются при беременности или желтухе в повышенных количествах. Это предположение подтвердилось, когда швейцарский химик Т. Рейхштейн и американский биохимик Э. Кендалл независимо друг от друга выделили кортикостероиды из коркового вещества надпочечников. Основным представителем глюкокортикостероидов (ГКС) в организме является кортизол, а кортизон - первый искусственно синтезированный ГКС - является
I Надежда Павловна Княжеская - доцент кафедры пульмонологии ФДПО ГБОУ ВПО "Российский национальный исследовательский медицинский университет им. Н.И. Пирогова" МЗ РФ, Москва.
продуктом его метаболизма. Работы Ф. Хенча, Э. Кендалла и Т. Рейхштейна были удостоены Нобелевской премии в 1950 г. .
Практически сразу после внедрения этих препаратов в клиническую практику было начато применение ГКС в лечении тяжелых форм бронхиальной астмы (БА), однако, несмотря на положительный ответ на терапию, их использование ограничивалось выраженными системными побочными эффектами: развитием стероидного васкулита, системного остеопороза, стероидного сахарного диабета, синдрома Иценко-Кушинга и т.д. Поэтому врачи и пациенты считали назначение ГКС крайней мерой, "терапией отчаяния". Попытки ингаляционного применения системных ГКС не увенчались успехом, поскольку независимо от способа введения этих препаратов сохранялись их системные осложнения, а терапевтический эффект при использовании небольших доз был недостаточным .
Практически сразу после создания системных ГКС встал вопрос о разработке их топических форм. Для этого потребовалось примерно 30 лет. Первое сообщение об успешном применении топических ГКС датировано 1971 г. и касалось применения беклометазона дипропионата при аллергическом рините, а в 1972 г. этот препарат был успешно использован в лечении БА. В настоящее время ингаляционные ГКС (ИГКС) являются базисными, т.е. основными, в терапии
всех патогенетических вариантов БА персисти-рующего течения, начиная с БА легкой степени тяжести, с учетом воспалительного генеза заболевания .
В это же время начинается активное изучение патофизиологических механизмов воспаления при БА, так как в 1970-х годах она приобретает статус одной из наиболее значимых проблем здравоохранения во всем мире. В настоящее время БА входит в число основных причин инвали-дизации и предотвратимой смерти, увеличивает общие расходы здравоохранения. Бронхиальную астму следует рассматривать прежде всего как хроническое заболевание с прогрессирующим развитием воспалительного процесса в дыхательных путях, что приводит к проявлению различных симптомов болезни в зависимости от степени воспаления (от незначительных до ярко выраженных).
В последние годы отмечен значительный прогресс в лечении БА. Это связано с определением БА как хронического воспалительного заболевания дыхательных путей и, вследствие этого, с широким применением ИГКС в качестве базисных противовоспалительных препаратов .
Роль ИГКС в лечении БА
В настоящее время ИГКС рассматриваются в качестве средств первой линии в терапии БА. Ингаляционные ГКС отличаются от системных своими фармакологическими свойствами: ли-пофильностью, быстротой инактивации, коротким периодом полувыведения из плазмы крови. Важно учитывать, что лечение ИГКС является местным (топическим), что обеспечивает выраженные противовоспалительные эффекты непосредственно в бронхиальном дереве. Противовоспалительный эффект ИГКС связан с их ин-гибирующим действием на клетки воспаления и их медиаторы, включая продукцию цитокинов, вмешательство в метаболизм арахидоновой кислоты и синтез лейкотриенов и простагландинов, снижение проницаемости микрососудов, предотвращение прямой миграции и активации клеток воспаления, повышение чувствительности Р-рецепторов гладкой мускулатуры. Ингаляционные ГКС повышают синтез противовоспалительных белков (липокортина-1), увеличивают апоптоз и снижают количество эозинофилов путем ингибирования интерлейкина-5. Таким образом, ИГКС способствуют стабилизации клеточных мембран, уменьшают проницаемость сосудов, улучшают функцию р-рецепторов, как путем синтеза новых рецепторов, так и путем повышения их чувствительности, стимулируют эпителиальные клетки .
Топические формы препаратов практически безопасны и не вызывают системных осложнений даже при длительном применении в высоких дозах . Тем не менее, как показывает опыт, назначение ИГКС по-прежнему вызывает опасения не только у пациентов, но и у врачей.
Важно своевременно поставить диагноз БА и верно определить тяжесть ее течения, зависящую от степени выраженности воспалительного процесса в бронхах, а затем подобрать необходимое противоастматическое лечение.
В Глобальной стратегии по лечению и профилактике бронхиальной астмы (Global Initiative for Asthma, GINA) пересмотра 2014 г. ИГКС рекомендованы уже на первой ступени терапии БА, сразу после постановки диагноза, так как достоверно известно, что даже при эпизодически возникающих симптомах БА в бронхиальном дереве прогрессирует воспаление, и, соответственно, раннее начало противовоспалительной терапии позволит быстрее и эффективнее достичь контроля БА. Ингаляционные ГКС как препараты для контроля БА (базисная терапия) следует применять ежедневно и длительно. Поэтому основное требование к этим препаратам заключается в том, что они должны быть не только эффективными, но и прежде всего безопасными.
Отдельное место в GINA 2014 г. занимает ком-плайнс пациента к проводимой терапии. В настоящее время лечение БА рассматривается как непрерывный цикл, и особое внимание уделяется вопросам техники ингаляции, которую нужно проверять на каждом визите, а также удовлетворенности от проводимой терапии. На сегодняшний день ни у кого не возникает сомнений, что приверженность пациентов к лечению играет одну из ведущих ролей в эффективности терапии БА. Следует разъяснять больным БА, что нельзя самостоятельно прекращать назначенное лечение при уменьшении и даже исчезновении симптомов заболевания без предварительной консультации с врачом. Если это условие не будет соблюдаться, то бесконтрольный воспалительный процесс будет прогрессировать, что приведет к учащению и нарастанию тяжести симптомов БА и обострений. Всё это повлечет за собой ухудшение качества жизни, возрастание недоверия пациента к врачам, ограничение физической активности, инвалидизацию и т.д.
В многочисленных рандомизированных пла-цебоконтролируемых исследованиях у больных БА продемонстрирована эффективность всех доз ИГКС в сравнении с плацебо (уровень доказательности А). В руководстве GINA 2002 г. было впервые введено понятие эквипотентных,
или эквивалентных доз, указывающее на то, что различные ИГКС отличаются друг от друга по степени противовоспалительного действия. Все ИГКС в эквипотентных дозах обладают противовоспалительным действием (уровень доказательности А) .
Отличительные свойства будесонида
Будесонид - высокоактивный препарат. Из всех ИГКС он имеет один из наиболее благоприятных терапевтических индексов, что связано с его высоким сродством к глюкокортикоидным рецепторам и ускоренным метаболизмом после системной абсорбции в легких и кишечнике. Для него доказана возможность однократного применения. Фактором, обеспечивающим возможность применения будесонида 1 раз в сутки, является ретенция будесонида в дыхательных путях посредством формирования внутриклеточного депо за счет обратимой этерификации (образования эфиров жирных кислот). При снижении концентрации свободного будесонида в клетке активируются внутриклеточные липазы, высвобождающийся из эфиров будесонид вновь связывается с глюкокортикоидным рецептором. В ряде исследований установлено, что внутриклеточное депонирование может оказаться более важным в плане активности препарата, чем сродство к рецептору .
Таким образом, будесонид обладает следующими свойствами:
Высокая эффективность: контроль симптомов БА у большинства пациентов;
Хороший профиль безопасности: отсутствие системных эффектов при использовании в терапевтических дозах. В исследованиях последних лет по изучению будесонида доказано, что он не влияет на конечный рост при длительном применении у детей, на минерализацию кости, катаракту, не вызывает ангиопатию;
Возможность применения у беременных. В проведенных исследованиях доказано, что его применение не вызывает увеличения числа аномалий плода ;
Возможность однократного применения: при назначении стандартных доз возможно использование препарата 1 раз в день;
Высокий комплайнс у пациентов, обусловленный удобным режимом дозирования и хорошей переносимостью.
Различные способы доставки ИГКС
Бесспорно, обязательным условием достижения противовоспалительного эффекта у пациентов с персистирующей БА является использование адекватных доз ИГКС. Однако следует заме-
тить, что для ИГКС точное и правильное выполнение дыхательного маневра является важным, как ни для одного другого ингаляционного препарата. Именно правильная техника ингаляции обеспечивает необходимую депозицию препарата в легких и способствует уменьшению местных нежелательных эффектов. При этом надо подчеркнуть, что ИГКС обладают минимальными побочными эффектами при правильном подборе и верной технике ингаляции. Наиболее часто наблюдаются местные нежелательные явления: кандидоз полости рта и ротоглотки, дисфония, иногда кашель, возникающий вследствие раздражения верхних дыхательных путей. Эти эффекты можно предотвратить, если использовать ингалятор с высоким уровнем доставки препарата в бронхиальное дерево. Таким образом, правильная техника ингаляции будет способствовать минимизации побочных эффектов со стороны ротоглотки. Поэтому правильный выбор ингаляционного устройства является неотъемлемым фактором успешной ингаляционной терапии. При выборе ингаляционного устройства необходимо учитывать предпочтения и особенности пациента, продолжительность терапии. При назначении пациенту ингаляционной терапии врач должен выбрать тот метод доставки и то устройство, которые больной хочет, может (способен выполнить указанный производителем ингаляционный маневр) и будет применять . В противном случае использование даже самого хорошего устройства станет пустой тратой времени и денег, будет утерян контроль над болезнью.
Врач, назначающий ингаляционные препараты, на каждом приеме должен проверять правильность выполнения ингаляционного маневра. К сожалению, нередки случаи, когда при назначении ингаляторов врачи не объясняют пациентам технику ингаляции и не проверяют ее правильность при последующих визитах.
Существуют различные типы систем доставки: дозированные аэрозольные ингаляторы (ДАИ), порошковые ингаляторы (ПИ), небулай-зеры. Каждое ингаляционное устройство имеет свои особенности и правила проведения ингаляции. Дозированные ингаляторы представлены ДАИ, активируемыми нажатием на баллончик, ДАИ, активируемыми вдохом пациента, и активируемыми вдохом ПИ.
Порошковые ингаляторы имеют ряд преимуществ перед аэрозольными: широкий возрастной диапазон применения, портативность, не содержат фреона. Они бывают мультидозовыми (многоразовыми) и однодозовыми. При использовании мультидозовых ПИ количество критических
ошибок (недополучение дозы) у пациентов значительно ниже, чем при использовании однодо-зовых ингаляторов . Важно подчеркнуть, что активируемые вдохом ПИ устраняют проблему координации вдоха и активации ингалятора, поэтому значительная доля частиц препарата попадает в легкие. Примером такого мультидозового устройства может служить ингалятор современного поколения Изихейлер.
Устройство доставки Изихейлер
Для пациентов при выборе ингаляционного устройства первостепенное значение имеет простота использования, в том числе доступно составленная инструкция по применению, компактный размер, привлекательный дизайн, удобный загубник, гигиеничность, а также наличие счетчика доз. При разработке Изихейлера ставилась задача обеспечить оптимальную приверженность пациентов лечению за счет дизайна, подобного ДАИ. Обязательными требованиями к Изихейлеру являлись простота и удобство применения, кроме того, ингаляционное устройство должно было функционировать независимо от характеристик потока вдыхаемого воздуха и обеспечивать доставку одинаковых доз от 1-й до 100-й (200-й) дозы.
Техника использования Изихейлера состоит из 6 шагов.
1. Снять крышку.
2. Встряхнуть ингалятор, держа его в вертикальном положении.
3. Нажать на верхнюю часть ингалятора до щелчка.
4. Сделать спокойный выдох, затем обхватить мундштук ингалятора губами и сделать глубокий вдох.
5. Если пациент должен получить несколько доз за одну ингаляцию, следует повторить все действия, начиная со второго шага.
6. По окончании ингаляции надеть крышку на ингалятор.
Преимущество Изихейлера заключается в доказанной многими исследователями стабильной доставке почти 100% вдыхаемой дозы даже при сниженном объеме вдоха, что особенно важно при лечении детей, лиц преклонного возраста и пациентов с тяжелым течением БА . Для активации большинства ПИ требуется определенный инспираторный поток (30 л/мин и более), в то время как для Изихейлера он может быть ниже 30 л/мин.
Изихейлер позволяет создать стабильную фракцию мелких частиц в высвобождаемой дозе лекарственного препарата и высокое депонирование препарата в дыхательных путях при до-
статочно широком диапазоне инспираторного усилия . Изихейлер обеспечивает лучшую доставку и распределение лекарственного вещества в легких по сравнению с аэрозольными ингаляторами, в том числе оснащенными спейсером .
Подавляющее большинство больных пришли к выводу, что научиться правильно пользоваться Изихейлером очень легко, причем это мнение встречалось одинаково часто среди пациентов разного возраста. При сравнении техники применения Изихейлера и других ингаляторов, которые больные использовали ранее, 88% детей, 86% подростков, 60% взрослых и 69% пожилых пациентов сообщили, что пользоваться Изихейлером гораздо легче. Только 8 больных испытали трудности при освоении Изихейле-ра по сравнению с другими ингаляторами . Спустя 3 мес применения Изихейлера больным был задан вопрос об их отношении к этому ингаляционному устройству. В целом 95% больных были довольны (52,7%) или очень довольны (42,7%) Изихейлером без значимой разницы между разными возрастными группами, хотя дети и подростки чаще, чем взрослые и пожилые пациенты, давали самую высокую оценку ингалятору . Больные БА лучше воспринимают Изихейлер, чем больные хронической обструктивной болезнью легких (ХОБЛ) (44,4% больных БА были довольны и 52,6% были очень довольны ингалятором по сравнению с 61,1 и 33,4% больных ХОБЛ соответственно) . Помимо опроса пациентов исследователи мони-торировали у них легочную функцию в качестве объективного критерия эффективности использования Изихейлера. Во всех группах основные параметры легочной функции (форсированная жизненная емкость легких, объем форсированного выдоха за 1-ю секунду и пиковая скорость выдоха) достоверно улучшились. Таким образом, в проведенных клинических исследованиях было продемонстрировано, что у больных разного возраста и с различными обструктивными бронхолегочными заболеваниями, с неудачным предшествующим опытом использования ПИ или в отсутствие опыта их использования перевод на Изихейлер не вызвал серьезных проблем, и в дальнейшем большинство пациентов отдавали предпочтение Изихейлеру. Особое значение описанные преимущества Изихейлера имеют именно для ИГКС. В России зарегистрирован Будесонид Изихейлер (Orion Pharma, Финляндия), который широко применяется в лечении БА и создает благоприятные условия для достижения контроля над заболеванием.
В проведенных исследованиях четко установлено, что применение устройства Изихейлер
является эффективным методом введения стандартных противоастматических лекарственных средств, включая Будесонид Изихейлер. Помимо терапевтической эквивалентности и сопоставимой с другими средствами доставки переносимости устройство Изихейлер обладает следующими характеристиками: стабильность дозы мелких частиц, устойчивая работоспособность независимо от скорости воздушного потока и предпочтения пациентов. Особенно важное значение имеет высокий процент пациентов, отдавших предпочтение Изихейлеру, поскольку это может влиять на приверженность лечению, а значит, и на клиническую эффективность .
Список литературы
Тер-Вартаньян С.Х. // Ревматология. http://rheumatology. org.ua/blog/articles/394
Лечение ревматических заболеваний ударными дозами ме-тилпреднизолона: Пособие для врачей / Под ред. В.А. Насоновой. Киев, 2009.
Современные аспекты глюкокортикоидной терапии ревматических заболеваний: Пособие для врачей / Под ред. В.А. Насоновой. Киев, 2009. Barnes N. // Eur. Respir. Rev. 1994. V. 4. P. 295. Цой А.Н. // Пульмонология. 1999. № 2. С. 73. Brattstrand R. // Eur. Respir. Rev. 1997. V. 7. P. 356. Global Initiative for Asthma. Workshop Report, 2014 // http://www.ginasthma.com/download.asp?intId=217 Barnes P.J. et al. // Am. J. Respir. Crit. Care Med. 1998. V. 157. № 3. Pt. 2. P. S1.
9. Barnes P.J. // J. Allergy Clin. Immunol. 1998. V. 102. № 4. Pt. 1. P. 531.
10. Adcock I.M. // Pulm. Pharmacol. Ther. 2000. V. 13. P. 115.
11. Rahman I., Mac Nee W. // Thorax. 1998. V. 53. P. 601.
12. Newton R. // Thorax. 2000. V. 55. P. 603.
13. Cox G. et al. // Am. J. Respir. Cell. Mol. Biol. 1991. V. 4. P. 525.
14. Lipworth B. // Arch. Intern. Med. 1999. V. 159. P. 941.
15. Глобальная стратегия лечения и профилактики бронхиальной астмы / Под ред. А.Г. Чучалина. М., 2002.
16. Miller-Larsson A. et al. // Drug Metab. Dispos. 1998. V. 26. P. 623.
17. Miller-Larsson A. et al. // Am. J. Respir. Crit. Care Med. 2000. V. 162. P. 1455.
18. Архипов В.В. и др. Заболевания легких при беременности / Под ред. А.Г. Чучалина и др. М., 2002.
19. Распопина Н.А. Бронхиальная астма при беременности: Автореф. ... дис. докт. мед. наук. М., 2004.
20. Van der Palen J. et al. // Eur. Respir. J. 1999. V. 14. P. 1034.
21. Lavorini F. et al. // Respir. Med. 2008. V. 102. P. 593.
22. Авдеев С.Н. // Рус. мед. журн. 2002. Т. 10. № 5. С. 255.
23. Laube B.L. et al. // Eur. Respir. J. 2011. V. 37. P. 1308.
24. Malmberg L.P. et al. // Int. J. Chron. Obstruct. Pulmon. Dis. 2010. V. 5. P. 257.
25. Панина Н.Т., Илькович М.М. // Тер. архив. 2013. № 3. С. 98.
26. Newman S.P. et al. // J. Aerosol Med. 2001. V. 14. P. 217.
27. Ahonen A. et al. // Curr. Ther. Res. Clin. Exp. 2000. V. 61. P. 61.
28. Белевский А.С. // Атмосфера. Пульмонология и аллергология. 2013. № 4. С. 31.
29. Galffy G. et al. // Drugs R. D. 2013. V. 13. P. 215.
30. Vanto T. et al. // J. Aerosol Med. 2004. V. 17. P. 15.
31. Schweisfurth H. et al. // Respir. Med. 2002. V. 96. P. 599.
Catad_tema Бронхиальная астма и ХОБЛ - статьи
Catad_tema Педиатрия - статьи
Л.Д. Горячкина, Н.И. Ильина, Л.С. Намазова, Л.М. Огородова, И.В. Сидоренко, Г.И. Смирнова, Б.А. Черняк
Главной целью лечения больных бронхиальной астмой является достижение и длительное поддержание контроля над заболеванием. Лечение должно начинаться с оценки текущего контроля над астмой, а объем терапии – регулярно пересматриваться, чтобы обеспечить достижение этого контроля.
Лечение бронхиальной астмы (БА) включает:
- Элиминационные мероприятия, направленные на уменьшение или исключение воздействия причинных аллергенов ().
- Фармакотерапию.
- Аллерген-специфическую иммунотерапию (АСИТ).
- Обучение больных.
ФАРМАКОТЕРАПИЯ
Для лечения БА у детей используют препараты, которые можно разделить на две большие группы:
- Средства базисной (поддерживающей, противовоспалительной) терапии.
- Симптоматические средства.
К препаратам базисной терапии относятся:
- лекарственные средства (ЛС) с противовоспалительным и/или профилактическим эффектом (глюкокортикостероиды (ГКС), антилейкотриеновые препараты, кромоны, анти-IgE-препараты);
- длительно действующие бронходилататоры (длительно действующие β 2 -адреномиметики, препараты теофиллина с медленным высвобождением).
Наибольшая клиническая и патогенетическая эффективность показана при использовании ингаляционных ГКС (ИГКС). Все средства базисной противовоспалительной терапии принимаются ежедневно и длительно. Принцип регулярности использования базисных препаратов позволяет достигать контроля над болезнью. Необходимо отметить, что в нашей стране для базисной терапии БА у детей с использованием комбинированных препаратов, содержащих ИГКС (с 12-часовым перерывом), зарегистрирован лишь режим стабильного дозирования. Другие схемы использования комбинированных препаратов у детей не разрешены.
К симптоматическим средствам относятся:
- ингаляционные короткодействующие β 2 -адреномиметики;
- антихолинергические препараты;
- препараты теофиллина с немедленным высвобождением;
- пероральные короткодействующие β 2 -адреномиметики.
Симптоматические препараты также называют средствами «скорой помощи». Их необходимо использовать для устранения бронхообструкции и сопутствующих ей острых симптомов (свистящие хрипы, чувство стеснения в груди, кашель). Данный режим применения лекарственных средств называется «по требованию».
ПУТИ ДОСТАВКИ ЛЕКАРСТВ
Препараты для лечения БА вводят различными путями: пероральным, парентеральным и ингаляционным (последний предпочтительнее). При выборе устройства для ингаляции учитывают эффективность доставки ЛС, стоимость/эффективность, удобство применения и возраст пациента (табл. 1). У детей для ингаляций используются три типа устройств: небулайзеры, дозирующие аэрозольные ингаляторы (ДАИ) и порошковые ингаляторы.
Таблица 1. Средства доставки лекарств при БА (возрастные приоритеты)
| Средство | Рекомендуемая возрастная группа |
Комментарии |
| Дозирующий аэрозольный ингалятор (ДАИ) | > 5 лет | Сложно координировать момент вдоха и нажатия на клапан баллончика (особенно детям). Около 80% дозы оседает в ротоглотке, необходимо полоскание полости рта после каждой ингаляции с целью снижения системной абсорбции |
| ДАИ, активируемый вдохом | > 5 лет | Применение данного средства доставки показано пациентам, не способным координировать момент вдоха и нажатия на клапан обычных ДАИ. Не может быть использован ни с одним из существующих спейсеров, кроме «оптимизатора» для данного типа ингаляторов |
| Порошковый ингалятор (ПИ) | ≥ 5 лет | При правильной технике использования эффективность ингаляции может быть выше, чем при применении ДАИ. Необходимо полоскать полость рта после каждого применения |
| Спейсер | > 4 лет < 4 лет при применении лицевой маски |
Использование спейсера снижает оседание препарата в ротоглотке, позволяет применять ДАИ с большей эффективностью, в случае наличия маски (в комплекте со спейсером) может быть использован у детей младше 4 лет |
| Небулайзер | < 2 лет (пациенты любого возраста, которые не могут использовать спейсер или спейсер/лицевую маску) |
Оптимальное средство доставки ЛС для использования в специализированных отделениях и отделениях интенсивной терапии, а также при оказании неотложной помощи, так как требует наименьших усилий от пациента и врача |
ПРОТИВОВОСПАЛИТЕЛЬНЫЕ (БАЗИСНЫЕ) ПРЕПАРАТЫ
I. Ингаляционные глюкокортикостероиды и комбинированные средства, содержащие ИГКС
В настоящее время ИГКС являются самыми эффективными препаратами для контроля БА, поэтому их рекомендуют для лечения персистирующей БА любой степени тяжести А. У детей школьного возраста, страдающих БА, поддерживающая терапия ИГКС позволяет контролировать симптомы БА, уменьшает частоту обострений и количество госпитализаций, повышает качество жизни, улучшает функцию внешнего дыхания, снижает гиперреактивность бронхов и уменьшает бронхоконстрикцию при физической нагрузке А. Применение ИГКС у детей дошкольного возраста, страдающих БА, приводит к клинически значимому улучшению состояния, включая балльную оценку дневного и ночного кашля, свистящего дыхания и одышки, физической активности, применения препаратов неотложного действия и использования ресурсов системы здравоохранения.
У детей применяют следующие ИГКС: беклометазон, флутиказон, будесонид. Дозы препаратов, используемых для базисной терапии, разделяют на низкие, средние и высокие. Прием ИГКС в низких дозах является безопасным, при назначении более высоких доз необходимо помнить о возможности развития побочных эффектов. Эквипотентные дозы, представленные в таблице 2, выработаны эмпирически, поэтому при выборе и смене ИГКС следует учитывать индивидуальные особенности пациента (ответ на терапию).
Таблица 2. Эквипотентные суточные дозы ИГКС
| Препарат* | Низкие суточные дозы (мкг) |
Средние суточные дозы (мкг) |
Высокие суточные дозы (мкг) |
|
Дозы для детей младше 12 лет |
|||
| Беклометазона дипропионат | 100–200 | > 200–400 | > 400 |
| Будесонид | 100–200 | > 200–400 | > 400 |
| Флутиказон | 100–200 | > 200–500 | > 500 |
|
Дозы для детей старше 12 лет |
|||
| Беклометазона дипропионат | 200–500 | > 500–1000 | > 1000–2000 |
| Будесонид | 200–400 | > 400–800 | > 800–1600 |
| Флутиказон | 100–250 | > 250–500 | > 500–1000 |
*Сопоставления препаратов основаны на данных об их сравнительной эффективности.
ИГКС входят в состав комбинированных препаратов для лечения БА. Такими препаратами являются Серетид (сальметерол + флутиказона пропионат) и Симбикорт (формотерол + будесонид). В большом количестве клинических исследований показано, что комбинация длительно действующих β 2 -адреномиметиков и ИГКС в низкой дозе более эффективна, чем увеличение дозы последнего. Комбинированная терапия сальметерол + флутиказон (в одном ингаляторе) способствует лучшему контролю БА, чем длительно действующий β 2 -адреномиметик и ИГКС в отдельных ингаляторах. На фоне длительной терапии сальметерол + флутиказон практически у каждого второго пациента можно достичь полного контроля БА (по данным исследования, включавшего пациентов в возрасте 12 лет и старше). Также отмечается значительное улучшение показателей эффективности терапии (ПСВ, ОФВ1, частоты обострений, качества жизни). В том случае, если применение низких доз ИГКС у детей не позволяет достичь контроля над БА, рекомендован переход на терапию комбинированным препаратом, что может быть хорошей альтернативой повышению дозы ИГКС. Это было показано в новом проспективном многоцентровом двойном слепом рандомизированном исследовании в параллельных группах продолжительностью 12 недель, где сравнивали эффективность комбинации сальметерол + флутиказон (в дозе 50/100 мкг 2 раза в сутки) и в 2 раза более высокой дозы флутиказона пропионата (200 мкг 2 раза в сутки) у 303 детей 4–11 лет с сохраняющимися симптомами БА, несмотря на предшествующую терапию низкими дозами ИГКС. Оказалось, что регулярное применение комбинации сальметерол + флутиказон (Серетид) предотвращает симптомы и обеспечивает достижение контроля над астмой так же эффективно, как и вдвое большая доза ИГКС. Лечение Серетидом сопровождается более выраженным улучшением функции легких и снижением потребности в препаратах для облегчения симптомов астмы при хорошей переносимости: в группе Серетида прирост утренней ПСВ на 46% выше, а число детей с полным отсутствием потребности в «спасательной терапии» на 53% больше, чем в группе флутиказона. Терапия с использованием комбинации формотерол + будесонид в составе одного ингалятора обеспечивает лучший контроль симптомов БА по сравнению с одним будесонидом у пациентов, у которых ранее ИГКС не обеспечивали контроля симптомов.
Влияние ИГКС на рост
Неконтролируемая или тяжелая БА замедляет рост детей и уменьшает итоговый рост. Ни в одном из продолжительных контролируемых исследований не показано никакого статистически или клинически значимого влияния на рост терапии ИКГ в дозе 100–200 мкг/сутки. Замедление линейного роста возможно при длительном назначении любого ИГКС в высокой дозе. Однако дети с БА, получающие ИГКС, достигают нормального роста, хотя иногда позднее, чем другие дети.
Влияние ИГКС на костную ткань
Ни в одном исследовании не было показано статистически значимого увеличения риска переломов костей у детей, получающих ИГКС.
Влияние ИГКС на гипоталамо-гипофизарно-надпочечниковую систему
Терапия ИГКС в дозе ИГКС и кандидоз полости рта
Клинически выраженная молочница отмечается редко и, вероятно, связана с сопутствующей терапией антибиотиками, применением высоких доз ИГКС и большой частотой ингаляций. Использование спейсеров и полоскание рта уменьшает частоту кандидоза.
Другие побочные эффекты
На фоне регулярной базисной противовоспалительной терапии не отмечено увеличения риска катаракты и туберкулеза.
II. Антагонисты лейкотриеновых рецепторов
Антилейкотриеновые препараты (зафирлукаст, монтелукаст) обеспечивают частичную защиту от бронхоспазма, вызванного физической нагрузкой, в течение нескольких часов после приема. Добавление антилейкотриеновых препаратов к лечению в случае недостаточной эффективности низких доз ИГКС обеспечивает умеренное клиническое улучшение, в том числе статистически значимое уменьшение частоты обострений. Клиническая эффективность терапии антилейкотриеновыми препаратами была показана у детей в возрасте > 5 лет при всех степенях тяжести БА, однако обычно эти препараты по эффективности уступают ИГКС в низких дозах. Антилейкотриеновые препараты можно использовать для усиления терапии у детей при среднетяжелой БА в тех случаях, когда заболевание недостаточно контролируется применением низких доз ИГКС. При использовании антагонистов лейкотриеновых рецепторов в качестве монотерапии у больных с тяжелой и среднетяжелой БА отмечают умеренное улучшение функции легких (у детей 6 лет и старше) и контроля БА (у детей 2 лет и старше) B . Зафирлукаст обладает умеренной эффективностью в отношении функции внешнего дыхания у детей 12 лет и старше со среднетяжелой и тяжелой БА А.
III. Кромоны
Недокромил и кромоглициевая кислота менее эффективна, чем ИГКС, в отношении клинических симптомов, функции внешнего дыхания, БА физического усилия, гиперреактивности дыхательных путей. Длительная терапия кромоглициевой кислотой при БА у детей по эффективности не отличается значительно от плацебо А. Недокромил, назначенный перед физической нагрузкой, позволяет уменьшить тяжесть и продолжительность вызванной ею бронхоконстрикции. Кромоны противопоказаны при обострении БА, когда требуется интенсивная терапия бронхорасширяющими препаратами быстрого действия. Роль кромонов в базисной терапии БА у детей (особенно у дошкольников) ограничена, в связи с отсутствием доказательств их эффективности. Проведенный в 2000 году метаанализ не позволил сделать однозначный вывод об эффективности кромоглициевой кислоты как средства базисной терапии БА у детей B . Следует помнить, что препараты данной группы не могут быть использованы для стартовой терапии среднетяжелой и тяжелой астмы. Применение кромонов в качестве базисной терапии возможно у пациентов с полным контролем симптомов БА. Кромоны не следует сочетать с β 2 -агонистами длительного действия, так как применение данных препаратов без ИГКС повышает риск смерти от астмы.
IV. Анти-IgE-препараты
Это принципиально новый класс ЛС, используемых сегодня для улучшения контроля над тяжелой персистирующей атопической БА. Омализумаб – наиболее изученный, первый и единственный рекомендованный к применению у детей старше 12 лет препарат. Высокая стоимость лечения омализумабом, а также необходимость ежемесячных визитов к врачу для инъекционного введения препарата оправданны у больных, нуждающихся в повторных госпитализациях, экстренной медицинской помощи, применяющих высокие дозы ингаляционных и/или системных ГКС.
V. Метилксантины длительного действия
Теофиллин значительно более эффективен, чем плацебо, для контроля БА и улучшения функции легких даже в дозах ниже обычно рекомендуемого терапевтического диапазонаА. Однако применение теофиллинов для лечения БА у детей проблематично из-за возможности тяжелых быстро возникающих (сердечная аритмия, смерть) и отсроченных (нарушение поведения, проблемы в обучении) побочных эффектов. В связи с чем применение теофиллинов возможно только под строгим фармакодинамическим контролем.
VI. Длительно действующие β 2 -агонисты Ингаляционные β 2 -адреномиметики длительного действия
Препараты этой группы эффективны для поддержания контроля БА (рис. 1). На постоянной основе их применяют только в комбинации с ИГКС и назначают только тогда, когда стандартные начальные дозы ИГКС не позволяют достичь контроля БА. Эффект этих препаратов сохраняется на протяжении 12 часов. Формотерол в виде ингаляций оказывает свое терапевтическое действие (расслабление гладкой мускулатуры бронхов) через 3 минуты, максимальный эффект развивается через 30–60 минут после ингаляции. Сальметерол начинает действовать относительно медленно, значимый эффект отмечают через 10–20 минут после ингаляции однократной дозы (50 мкг), а эффект, сопоставимый с таковым после приема сальбутамола, развивается через 30 минут. Из-за медленного начала действия сальметерол не следует назначать для купирования острых симптомов БА. Так как действие формотерола развивается быстрее, чем действие сальметерола, это позволяет использовать формотерол не только для профилактики, но и для купирования симптомов БА. Однако, согласно рекомендациям GINA 2006, длительнодействующие β 2 -адреномиметики могут быть использованы только у больных, уже получающих регулярную поддерживающую терапию ИГКС.
Рисунок 1. Классификация β 2 -агонистов

Дети хорошо переносят лечение ингаляционными β 2 -адреномиметиками длительного действия даже при продолжительном применении, а их побочные эффекты сопоставимы с таковыми β 2 -адреномиметиков короткого действия (в случае их применения по требованию). Препараты данной группы следует назначать только совместно с базисной терапией ИГКС, так как монотерапия β 2 -адреномиметиками длительного действия без ИГКС увеличивает вероятность смерти больных! Вследствие противоречивых данных о влиянии на обострения БА эти средства не являются препаратами выбора для пациентов, нуждающихся в назначении двух и более средств поддерживающей терапии.
Пероральные β 2 -адреномиметики длительного действия
Препараты этой группы включают лекарственные формы сальбутамола длительного действия. Эти ЛС могут помочь в контроле ночных симптомов БА. Их можно использовать в дополнение к ИГКС, если последние в стандартных дозах не обеспечивают достаточного контроля ночных симптомов. Возможные побочные эффекты включают стимуляцию сердечно-сосудистой системы, тревогу и тремор. В нашей стране в педиатрии препараты данной группы используются редко.
VII. Антихолинергические препараты
Ингаляционные антихолинергические средства не рекомендованы для длительного применения (базисной терапии) у детей с БА.
VIII. Системные ГКС
Несмотря на то что системные ГКС эффективны в отношении БА, необходимо учитывать развитие нежелательных явлений при длительной терапии, таких как угнетение гипоталамо-гипофизарно-надпочечниковой системы, увеличение массы тела, стероидный диабет, катаракта, АГ, задержка роста, иммунносупрессия, остеопороз, психические расстройства. Учитывая риск побочных эффектов при длительном применении, пероральные ГКС следует использовать у детей с астмой только в случае развития тяжелых обострений, как на фоне вирусной инфекции, так и в ее отсутствие.
СРЕДСТВА НЕОТЛОЖНОЙ ТЕРАПИИ
Ингаляционные β 2 -адреномиметики быстрого действия (короткодействующие β 2 -агонисты) самые эффективные из существующих бронхолитиков, они являются препаратами выбора для лечения острого бронхоспазма А (рис. 1). К данной группе препаратов относятся сальбутамол, фенотерол и тербуталин (табл. 3).
Таблица 3. Препараты неотложной помощи при БА
| Препарат | Доза | Побочные эффекты | Комментарии |
|
β 2 -адреномиметики |
|||
| Сальбутамол (ДАИ) | 1 доза – 100 мкг По 1–2 ингаляции до 4 раз в день |
Тахикардия, тремор, головная боль, раздражительность |
Рекомендованы только в режиме «по требованию» |
| Сальбутамол (раствор для небулайзерной терапии) |
2,5 мг/2,5 мл | ||
| Фенотерол (ДАИ) | 1 доза – 100 мкг По 1–2 ингаляции до 4 раз в день |
||
| Фенотерол (раствор для небулайзерной терапии) |
1 мг/мл | ||
|
Антихолинергические препараты |
|||
| Ипратропия бромид (ДАИ) с 4 лет | 1 доза – 20 мкг По 2–3 ингаляции до 4 раз в день |
Незначительная сухость и неприятный вкус во рту |
Преимущественно применяется у детей до 2 лет |
| Ипратропия бромид (раствор для небулайзерной терапии) | 250 мкг/мл | ||
|
Комбинированные препараты |
|||
| Фенотерол + ипратропия бромид (ДАИ) | По 2 ингаляции до 4 раз в день | Тахикардия, тремор, головная боль, раздражительность, незначительная сухость и неприятный вкус во рту |
Характерны побочные эффекты, указанные для каждого из входящих в состав комбинации средств |
| Фенотерол + ипратропия бромид (раствор для небулайзерной терапии) |
1–2 мл | ||
|
Теофиллин короткого действия |
|||
| Эуфиллин в любой лекарственной форме | 150 мг > 3 лет по 12–24 мг/кг/сут |
Тошнота, рвота, головная боль, тахикардия, нарушения сердечного ритма |
В настоящее время Использование эуфиллина у детей для купирования симптомов БА не оправдано |
Антихолинергические средства имеют ограниченную роль в лечении БА у детей. В метаанализе исследований ипратропиума бромида в комбинации с β 2 -агонистами при обострении БА показано, что применение антихолинергического препарата сопровождается статистически значимым (хотя и умеренным) улучшением функции легких и снижением риска госпитализации.
ДОСТИЖЕНИЕ КОНТРОЛЯ НАД АСТМОЙ
В процессе лечения должна проводиться постоянная оценка и коррекция терапии на основе изменений уровня контроля над астмой. Весь цикл терапии включает:
- оценку уровня контроля над БА;
- лечение, направленное на достижение контроля;
- лечение с целью поддержания контроля.
Оценка уровня контроля над БА
Контроль над БА является комплексным понятием, включающим совокупность следующих показателей:
- минимальное количество или отсутствие (≤ 2 эпизодов в неделю) дневных симптомов БА;
- отсутствие ограничений в повседневной активности и физических нагрузках;
- отсутствие ночных симптомов и пробуждений из-за БА;
- минимальная потребность или отсутствие потребности (≤ 2 эпизодов в неделю) в бронхолитиках короткого действия;
- нормальные или практически нормальные показатели функции легких;
- отсутствие обострений БА.
В соответствии с GINA 2006, выделяют три уровня контроля над БА: контролируемую, частично контролируемую и неконтролируемую БА. В настоящее время разработано несколько инструментов для интегральной оценки уровня контроля над БА. Одним из таких инструментов является Тест по контролю над бронхиальной астмой у детей (Childhood Asthma Control Test) в возрасте 4–11 лет – валидизированный опросник, позволяющий врачу и пациенту (родителю) быстро оценить выраженность проявлений БА и потребность в увеличении объема терапии. Тест состоит из 7 вопросов, причем вопросы 1–4 предназначены для ребенка (4-балльная оценочная шкала ответов: от 0 до 3 баллов), а вопросы 5–7 – для родителей (6-балльная шкала: от 0 до 5 баллов). Результатом теста является сумма оценок за все ответы в баллах (максимальная оценка – 27 баллов). Оценка 20 баллов и выше соответствует контролируемой астме, 19 баллов и ниже означает, что астма контролируется недостаточно эффективно; пациенту рекомендуется воспользоваться помощью врача для пересмотра плана лечения. В этом случае необходимо также расспросить ребенка и его родителей о препаратах для ежедневного применения, чтобы убедиться в правильности техники ингаляций и соблюдении режима лечения. Осуществить тестирование по контролю над астмой можно на сайте www.astmatest.ru.
Лечение, направленное на поддержание контроля
Выбор медикаментозной терапии зависит от текущего уровня контроля над астмой и текущей терапии пациента. Так, если текущая терапия не обеспечивает контроля над БА, необходимо увеличивать объем терапии (переходить на более высокую ступень) до достижения контроля. В случае сохранения контроля над БА в течение 3 месяцев и более возможно уменьшение объема поддерживающей терапии с целью достижения минимального объема терапии и наименьших доз препаратов, достаточных для поддержания контроля. В случае достижения частичного контроля над БА следует рассмотреть возможность увеличения объема терапии с учетом наличия более эффективных подходов к лечению (т.е. возможности увеличения доз или добавления других препаратов), их безопасности, стоимости и удовлетворенности пациента достигнутым уровнем контроля.
Большинство препаратов для лечения БА отличаются благоприятными сочетаниями польза/риск по сравнению со средствами для лечения других хронических заболеваний. Каждая ступень включает варианты терапии, которые могут служить альтернативами при выборе поддерживающей терапии БА, хотя и не являются одинаковыми по эффективности. Объем терапии возрастает от ступени 2 к ступени 5; хотя на ступени 5 выбор лечения зависит также от доступности и безопасности лекарственных препаратов. У большинства больных с симптомами персистирующей БА, ранее не получавших поддерживающей терапии, лечение следует начинать со ступени 2. Если симптомы БА при первичном осмотре чрезвычайно выражены и указывают на отсутствие контроля, лечение необходимо начинать со ступени 3 (табл. 4). На каждой ступени терапии пациенты должны использовать препараты для быстрого облегчения симптомов БА (бронходилататоры быстрого действия). Однако регулярное использование препаратов для облегчения симптомов является одним из признаков неконтролируемой БА, указывающим на необходимость увеличения объема поддерживающей терапии. Поэтому уменьшение или отсутствие потребности в препаратах неотложной терапии является важной целью лечения и критерием эффективности терапии.
Таблица 4. Соответствие ступеней терапии клиническим характеристикам БА
| Ступени терапии | Клиническая характеристика пациентов |
| Ступень 1 | Кратковременные (до нескольких часов) симптомы БА в дневное время (кашель, свистящие хрипы, одышка возникающие ≤ 2 раз в неделю или еще более редкие ночные симптомы). В межприступный период – отсутствуют проявления БА и ночные пробуждения, функция легких в пределах нормы. ПСВ ≥ 80% от должных значений |
| Ступень 2 | Симптомы БА чаще 1 раза в неделю, но реже 1 раза в день. Обострения могут нарушать активность пациентов и ночной сон. Ночные симптомы чаще 2 раз в месяц. Функциональные показатели внешнего дыхания в пределах возрастной нормы. В межприступный период – отсутствуют проявления БА и ночные пробуждения, переносимость физической нагрузки не снижена. ПСВ ≥ 80% от должных значений |
| Ступень 3 | Симптомы БА отмечаются ежедневно. Обострения нарушают физическую активность ребенка и ночной сон. Ночные симптомы чаще 1 раза в неделю. В межприступном периоде отмечаются эпизодические симптомы, сохраняются изменения функции внешнего дыхания. Переносимость физической нагрузки может быть снижена. ПСВ 60–80% от должных значений |
| Ступень 4 | Частое (несколько раз в неделю или ежедневно, по несколько раз в день) появление симптомов БА, частые ночные приступы удушья. Частые обострения заболевания (1 раз в 1–2 месяца). Ограничение физической активности и выраженные нарушения функции внешнего дыхания. В периоде ремиссии сохраняются клинико-функциональные проявления бронхиальной обструкции. ПСВ ≤ 60% от должных значений |
| Ступень 5 | Ежедневные дневные и ночные симптомы, по несколько раз в день. Выраженное ограничение физической активности. Выраженные нарушения функции легких. Частые обострения (1 раз в месяц и чаще). В периоде ремиссии сохраняются выраженные клинико-функциональные проявления бронхиальной обструкции. ПСВ < 60% от должных значений |
Ступень 1 , включающая применение препаратов для облегчения симптомов по потребности, предназначена только для пациентов, не получавших поддерживающей терапии. В случае более частого появления симптомов или эпизодического ухудшения состояния пациентам показана регулярная поддерживающая терапия (в дополнение к препаратам для облегчения симптомов по потребности.
Ступени 2–5 включают комбинацию препарата для облегчения симптомов (по потребности) с регулярной поддерживающей терапией. В качестве начальной поддерживающей терапии БА у больных любого возраста на ступени 2 рекомендуются ИГКС в низкой дозе. Альтернативными средствами являются ингаляционные антихолинергические препараты, пероральные β 2 -агонисты короткого действия или теофиллин короткого действия. Однако для этих препаратов характерно более медленное начало действия и более высокая частота побочных эффектов.
На ступени 3 рекомендуется назначать комбинацию ИГКС в низкой дозе с ингаляционным (β 2 -агонистом длительного действия в виде фиксированной комбинации. Благодаря аддитивному эффекту комбинированной терапии пациентам обычно оказывается достаточно назначения низких доз ИГКС; увеличение дозы ИГКС требуется только пациентам, у которых контроль над БА не был достигнут через 3–4 месяца терапии. Показано, что β 2 -агонист длительного действия формотерол, для которого характерно быстрое начало действия при применении в виде монотерапии или в составе фиксированной комбинации с будесонидом, не менее эффективен для купирования острых проявлений БА, чем β 2 -агонисты короткого действия. Однако монотерапия формотеролом для облегчения симптомов не рекомендуется, и этот препарат должен всегда использоваться только вместе с ИГКС. У всех детей, а в особенности у детей в возрасте 5 лет и младше, комбинированная терапия изучена в меньшей степени, чем у взрослых. Однако в недавнем исследовании показано, что добавление β 2 -агониста длительного действия более эффективно, чем увеличение дозы ИГКС. Вторым вариантом терапии является увеличение доз ИГКС до средних доз. Больным любого возраста, получающим средние или высокие дозы ИГКС с помощью ДАИ, рекомендовано применение спейсера для улучшения доставки препарата в дыхательные пути, снижения риска орофарингеальных побочных эффектов и системной абсорбции препарата. Еще одним альтернативным вариантом терапии на ступени 3 является комбинация ИГКС в низкой дозе с антилейкотриеновым препаратом. Вместо антилейкотриенового препарата возможно назначение низкой дозы теофиллина замедленного высвобождения. Эти варианты терапии не исследовались у детей в возрасте 5 лет и младше.
Выбор препаратов на ступени 4 зависит от предшествующих назначений на ступенях 2 и 3. Однако порядок добавления дополнительных препаратов должен быть основан на доказательствах их сравнительной эффективности, полученных в клинических исследованиях. Больных, у которых не был достигнут контроль над БА на ступени 3, следует направлять (если есть возможность) к специалисту в области лечения БА с целью исключения альтернативных диагнозов и/или причин БА, трудно поддающейся терапии. Предпочтительным подходом к лечению на ступени 4 является использование комбинации ГКС в средней или высокой дозе с ингаляционным β 2 -агонистом длительного действия. Длительное применение ИГКС в высоких дозах сопровождается повышенным риском развития побочных эффектов.
Терапия ступени 5 требуется пациентам, у которых не достигнут эффект лечения на фоне применения высоких доз ИГКС в комбинации с β 2 -агонистами длительного действия и другими препаратами для поддерживающей терапии. Добавление перорального ГКС к другим препаратам для поддерживающей терапии может увеличивать эффект лечения, но сопровождается тяжелыми нежелательными явлениями. Больной должен быть предупрежден о риске развития побочных эффектов; также необходимо рассмотреть возможность всех других альтернатив терапии БА.
Схемы уменьшения объема базисной терапии БА
Если контроль над БА достигнут на фоне базисной терапии комбинацией ИГКС и β 2 -агониста длительного действия и поддерживается не менее 3 месяцев, можно начинать постепенное уменьшение ее объема: снижения дозы ИГКС не более чем на 50% в течение 3 месяцев при продолжении терапии β 2 -агонистом длительного действия. При сохранении полного контроля на фоне терапии низкими дозами ИГКС и β 2 -агонистом длительного действия 2 раза в сутки следует отменить последний и продолжать терапию ИГКСB. Достижение контроля на фоне применения кромонов не требует редукции их дозы.
Другая схема уменьшения объема базисной терапии у больных, получающих ИГКС и β 2 -агонист длительного действия и, предполагает отмену последнего на первом этапе при продолжении монотерапией ИГКС в такой же дозе, какая содержалась в фиксированной комбинации. В последующем постепенно снижать дозу ИГКС не более чем на 50% в течение 3 месяцев при условии сохранения полного контроля над БА. Монотерапия β 2 -агонистом длительного действия без ИГКС недопустима, так как может сопровождаться увеличением риска смерти больных БА. Прекращение поддерживающей терапии возможно, если полный контроль над БА сохраняется при использовании минимальной дозы противовоспалительного препарата, отсутствии рецидива симптомов в течение одного года D .
При уменьшении объема противовоспалительной терапии следует учитывать спектр чувствительности пациентов к аллергенам. Например, перед сезоном цветения у пациентов с БА и пыльцевой сенсибилизацией категорически нельзя уменьшать дозы применяемых базисных средств, напротив, объем противовоспалительной терапии на этот период следует увеличить!
Увеличение объема базисной терапии в ответ на утрату контроля над астмой
Объем терапии следует увеличивать при утрате контроля над БА (увеличении частоты и тяжести симптомов БА, потребности в ингаляции β 2 -агонистов в течение 1–2 дней, снижении показателей пикфлоуметрии или ухудшении переносимости физической нагрузки). Объем терапии БА регулируется в течение года в соответствии со спектром сенсибилизации причиннозначимых аллергенов. Для купирования у больных БА остро возникших нарушений бронхиальной проходимости используют сочетание бронхолитических (β 2 -агонисты, антихолинергические препараты, метилксантины) и ГКС препаратов. Предпочтение следует отдавать ингаляционным формам доставки, позволяющим достичь быстрого эффекта при минимальном общем воздействии на организм ребенка.
Имеющиеся рекомендации по уменьшению доз различных препаратов базисной терапии могут иметь достаточно высокий уровень доказательности (преимущественно B), но основываются на данных исследований, в которых оценивали только клинические показатели (симптомы, ОФВ1) и не определяли влияние уменьшенного объема терапии на активность воспаления и структурные изменения при астме. Таким образом, рекомендации по снижению объема терапии требуют проведения дальнейших исследований, направленных на оценку процессов, лежащих в основе заболевания, а не только клинических проявлений.
ОБУЧЕНИЕ ПАЦИЕНТА
Образование является необходимой составной частью комплексной программы лечения детей с БА, и подразумевает установление партнерства между пациентом, его семьей и медицинским работником.
Задачи образовательных программ:
- информирование о необходимости элиминационных мероприятий;
- обучение технике использования ЛС;
- информирование об основах фрамакотерапии;
- обучение мониторингу симптомов заболевания, пикфлуометрии (у детей старше 5 лет), ведению дневника самоконтроля;
- составлению индивидуального плана действий при обострении.
ПРОГНОЗ
У детей с повторяющимися эпизодами свистящих хрипов на фоне ОРВИ, не имеющих признаков атопии и атопических заболеваний в семейном анамнезе, симптомы БА обычно исчезают в дошкольном возрасте и в дальнейшем не развиваются, хотя могут сохраняться минимальные изменения функции легких и бронхиальная гиперреактивность. При возникновении свистящих хрипов в раннем возрасте (до 2 лет) в отсутствие других проявлений семейной атопии вероятность того, что симптомы будут сохраняться и в более позднем возрасте, невелика. У детей раннего возраста с частыми эпизодами свистящих хрипов, БА в семейном анамнезе и проявлениями атопии, риск развития БА в возрасте 6 лет значительно увеличивается. Мужской пол является фактором риска для возникновения БА в препубертатном периоде, однако существует большая вероятность того, что по достижению взрослого возраста заболевание исчезнет. Женский пол является фактором риска персистирования БА во взрослом возрасте.
Людмила Александровна Горячкина , заведующая кафедрой аллергологии ГОУ ДПО «Российская медицинская академия последипломного образования» Росздрава, профессор, д-р мед. наук
Наталья Ивановна Ильина , главный врач ГНЦ РФ «Институт иммунологии» ФМБА, профессор, д-р мед. наук, заслуженный врач РФ
Лейла Сеймуровна Намазова , директор НИИ профилактической педиатрии и восстановительного лечения ГУ Научного центра здоровья детей РАМН, заведующая кафедрой аллергологии и клинической иммунологии ФППО педиатров ГОУ ВПО «Московская медицинская академия им. И.М. Сеченова» Росздрава, член Исполкома Союза педиатров России и Европейского общества педиатров, профессор, д-р мед. наук, главный редактор журнала «Педиатрическая фармакология»
Людмила Михайловна Огородова , проректор по научной работе и последипломной подготовке, заведующая кафедрой факультетской педиатрии с курсом детских болезней лечебного факультета ГОУ ВПО «Сибирская государственная медицинская академия» Росздрава, член-корреспондент РАМН, д-р мед. наук, профессор
Ирина Валентиновна Сидоренко , главный аллерголог комитета здравоохранения г. Москвы, доцент, канд. мед. наук
Галина Ивановна Смирнова , профессор, кафедра педиатрии ГОУ ВПО «Московская медицинская академия им. И.М. Сеченова» Росздрава, д-р мед. наук
Борис Анатольевич Черняк , заведующий кафедрой аллергологии и пульмонологии, ГОУ ДПО «Иркутский государственный институт усовершенствования врачей» Росздрава
Для цитирования:
Княжеская Н.П. Глюкокортикостероиды в терапии бронхиальной астмы // РМЖ. 2002. №5. С. 245
Кафедра пульмонологии ФУВ РГМУ
В последние годы отмечен значительный прогресс в лечении бронхиальной астмы (БА) . По-видимому, это связано с определением БА, как хронического воспалительного заболевания дыхательных путей, и вследствие этого - с широким применением ингаляционных глюкокортикостероидов (ГКС) в качестве базисных противовоспалительных препаратов. Однако несмотря на достигнутые успехи, уровень контроля над течением заболевания нельзя считать удовлетворительным. Так, например, почти каждый третий больной БА, как минимум, 1 раз в месяц просыпается ночью в связи с симптомами болезни. Более половины больных имеют ограничения физической активности, более трети вынуждены пропускать занятия в школе или отсутствовать на работе. Более 40% больных вынуждены обращаться за неотложной помощью вследствие обострения заболевания. Причины подобной ситуации многообразны, и не последнюю роль в этом играет недостаточная осведомленность врача в патогенезе БА и, соответственно, выбор неправильной тактики лечения.
Определение и классификация БА
Бронхиальная астма - хроническое заболевание дыхательных путей, в котором принимают участие многие клетки: тучные клетки, эозинофилы и Т-лимфоциты. У предрасположенных лиц это воспаление приводит к повторным эпизодам хрипов, одышки, тяжести в грудной клетке и кашлю, особенно ночью и/или ранним утром. Эти симптомы сопровождаются распространенной, но вариабельной обструкцией бронхиального дерева, которая, по крайней мере, частично обратима, спонтанно или под влиянием лечения. Воспаление также вызывает увеличение ответа дыхательных путей на различные стимулы (гиперреактивность).
Ключевыми положениями определения следует считать следующие:
1. БА - хроническое персистирующее воспалительное заболевание дыхательных путей вне зависимости от тяжести течения.
2. Воспалительный процесс приводит к гиперреактивности бронхов, обструкции и появлению респираторных симптомов.
3. Обструкция дыхательных путей обратима, по крайней мере, частично.
4. Атопия - генетическая предрасположенность к продукции иммуноглобулинов класса Е (может присутствовать не всегда).
Бронхиальную астму можно классифицировать на основе этиологии, тяжести течения и особенностей проявления бронхиальной обструкции.
Однако в настоящее время бронхиальную астму в первую очередь следует классифицировать по степени тяжести, т. к. именно это отражает степень выраженности воспалительного процесса в дыхательных путях и определяет тактику противовоспалительной терапии.
Степень тяжести определяется по следующим показателям:
- Количество ночных симптомов в неделю.
- Количество дневных симптомов в день и в неделю.
- Кратность применения b 2 -агонистов короткого действия.
- Выраженность нарушений физической активности и сна.
- Значения пиковой скорости выдоха (ПСВ) и ее процентное соотношение с должным или наилучшим значением.
- Суточные колебания ПСВ.
- Объем проводимой терапии.
Существует 5 степеней тяжести течения БА: легкая интермиттирующая; легкая персистирующая; средней тяжести персистирующая; тяжелая персистирующая; тяжелая персистирующая стероидозависимая (табл. 1).
БА интермиттирующего течения: симптомы астмы реже 1 раза в неделю; короткие обострения (от нескольких часов до нескольких дней). Ночные симптомы 2 раза в месяц или реже; отсутствие симптомов и нормальная функция легких между обострениями: пиковая скорость выдоха (ПСВ) > 80% от должного и колебания ПСВ менее 20%.БА легкого персистирующего течения . Симптомы 1 раз в неделю или чаще, но реже 1 раза в день. Обострения заболевания могут нарушать активность и сон. Ночные симптомы возникают чаще 2 раз в месяц. ПСВ более 80% от должного; колебания ПСВ 20-30%.
БА средней тяжести . Ежедневные симптомы. Обострения нарушают активность и сон. Ночные симптомы возникают более 1 раза в неделю. Ежедневный прием b 2 -агонистов короткого действия. ПСВ 60-80% от должного. Колебания ПСВ более 30%.
БА тяжелого течения: постоянные симптомы, частые обострения, частые ночные симптомы, физическая активность ограничена проявлениями астмы. ПСВ менее 60% от должного; колебания более 30%.
Необходимо отметить, что определение степени тяжести астмы по этим показателям возможно только перед началом лечения. Если больной уже получает необходимую терапию, то ее объем также должен учитываться. Таким образом, если у пациента по клинической картине определяется легкая персистирующая астма, но при этом он получает медикаментозное лечение, соответствующее тяжелой персистирующей астме, то у данного пациента диагностируется БА тяжелого течения.
БА тяжелого течения стероидозависимая: независимо от клинической картины пациент, получающий длительное лечение системными кортикостероидами, должен быть расценен, как страдающий БА тяжелого течения.
Ингаляционные ГКС
Рекомендован ступенчатый подход к терапии БА
в зависимости от тяжести ее течения (табл. 1). Все препараты для лечения БА разделены на две основные группы: для длительного контроля воспалительного процесса и средства для купирования острых симптомов астмы. Основой терапии для длительного контроля воспалительного процесса являются ингаляционные глюкокортикостероиды (ИГКС), которые следует применять, начиная со второй ступени (легкое персистирующее течение) до пятой (тяжелое стероидозависимое течение). Поэтому в настоящее время ИГКС рассматриваются в качестве средств первой линии для терапии БА. Чем выше степень тяжести течения БА, тем большие дозы ИГКС следует применять. По данным ряда исследований, у пациентов, начавших лечение ИГКС не позже двух лет от начала заболевания, отмечены существенные преимущества в улучшении контроля над симптомами астмы по сравнению с группой, начавшей лечение ИГКС по прошествии более чем 5 лет от дебюта заболевания.
Механизмы действия и фармакокинетика
ИГКС способны связываться со специфическими рецепторами в цитоплазме, активируют их и образуют с ними комплекс, который затем димеризуется и перемещается в ядро клетки, где связывается с ДНК и взаимодействует с механизмами транскрипции ключевых ферментов, рецепторов и других сложных белков. Это приводит к проявлению фармакологического и терапевтического действия.
Противовоспалительный эффект ИГКС связан с их ингибирующим действием на клетки воспаления и их медиаторы, включая продукцию цитокинов, вмешательство в метаболизм арахидоновой кислоты и синтез лейкотриенов и простагландинов, предотвращение миграции и активации клеток воспаления. ИГКС увеличивают синтез противовоспалительных белков (липокортина-1), увеличивают апоптоз и снижают количество эозинофилов путем ингибирования интерлейкина-5. Таким образом, ИГКС приводят к стабилизации клеточных мембран, уменьшают проницаемость сосудов, улучшают функцию b -рецепторов как путем синтеза новых, так и повышая их чувствительность, стимулируют эпителиальные клетки.
ИГКС отличаются от системных глюкокортикостероидов своими фармакологическими свойствами: липофильностью, быстротой инактивации, коротким периодом полувыведения из плазмы крови. Важно учитывать, что лечение ИГКС является местным (топическим), что обеспечивает выраженные противовоспалительные эффекты непосредственно в бронхиальном дереве при минимальных системных проявлениях. Количество ИГКС, доставляемое в дыхательные пути, зависит от номинальной дозы препарата, типа ингалятора, наличия или отсутствия пропеллента, а также техники выполнения ингаляции. До 80% пациентов испытывают сложности при использовании дозированных аэрозолей.
Наиболее важной характеристикой для проявления селективности и времени задержки препарата в тканях является липофильность . Благодаря липофильности ИГКС накапливаются в дыхательных путях, замедляется их высвобождение из тканей и увеличивается их сродство к глюкокортикоидному рецептору. Высоколипофильные ИГКС быстрее и лучше захватываются из просвета бронхов и длительно задерживаются в тканях дыхательных путей. ИГКС отличает от системных препаратов их топическое (местное) действие. Поэтому бесполезно назначать ингаляции системных ГКС (гидрокортизона, преднизолона и дексаметазона): эти препараты вне зависимости от способа применения обладают только системным действием.
В многочисленных рандомизированных плацебо-контролируемых исследованиях у больных БА показана эффективность всех доз ИГКС в сравнении с плацебо.
Системная биодоступность складывается из пероральной и ингаляционной. От 20 до 40% от ингалируемой дозы препарата попадает в дыхательные пути (это величина значительно варьирует в зависимости от средства доставки и от ингаляционной техники пациента). Легочная биодоступность зависит от процента попадания препарата в легкие, наличия или отсутствия носителя (лучшие показатели имеют ингаляторы, не содержащие фреон) и от абсорбции препарата в дыхательных путях. 60-80% ингаляционной дозы оседает в ротоглотке и проглатывается, подвергаясь затем полному или частичному метаболизму в желудочно-кишечном тракте и печени. Пероральная доступность зависит от абсорбции в желудочно-кишечном тракте и от выраженности эффекта «первого прохождения» через печень, благодаря чему в системный кровоток поступают уже неактивные метаболиты (за исключением беклометазона 17-монопропионата - активного метаболита беклометазона дипропионата). Дозы ИГКС до 1000 мкг/сутки (для флютиказона до 500 мкг/сут) обладают незначительным системным действием.
Все ИГКС имеют быстрый системный клиренс , сравнимый с величиной печеночного кровотока. Это один из факторов, снижающих системное действие ИГКС.
Характеристика наиболее часто используемых препаратов
К ИГКС относятся беклометазона дипропионат, будесонид, флютиказона пропионат, флунизолид, триамсинолона ацетонид, мометазона фуроат. Они выпускаются в виде дозированных аэрозолей, порошковых ингаляторов, а также в виде растворов для ингаляции через небулайзер (будесонид).
Беклометазона дипропионат . Применяется в клинической практике более 20 лет и остается одним из самых эффективных и часто используемых препаратов. Разрешено применение препарата у беременных. Выпускается в виде дозированного аэрозольного ингалятора (Бекотид 50 мкг, Беклофорте 250 мкг, Альдецин 50 мкг, Беклокорт 50 и 250 мкг, Бекломет 50 и 250 мкг/доза), дозированного ингалятора, активируемого вдохом (Беклазон Легкое Дыхание 100 и 250 мкг/доза), порошкового ингалятора (Бекодиск 100 и 250 мкг/доза ингалятор Дискхалер; мультидозовый ингалятор Изихейлер, Бекломет 200 мкг/доза). Для ингаляторов Бекотид и Беклофорте производятся специальные спейсеры - «Волюматик» (клапанный спейсер большого объема для взрослых) и «Бэбихалер» (2-клапанный спейсер малого объема с силиконовой лицевой маской для детей раннего возраста).
Будесонид . Современный высокоактивный препарат. Используется в виде дозированного аэрозольного ингалятора (Будесонид-мите 50 мкг/доза; Будесонид-форте 200 мкг/доза), порошкового ингалятора (Пульмикорт Турбухалер 200 мкг/доза; Бенакорт Циклохалер 200 мкг/доза) и суспензии для небулайзера (Пульмикорт 0,5 и 0,25 мг/доза). Пульмикорт Турбухалер - единственная лекарственная форма ИГКС, не содержащая носителя. Для дозированных ингаляторов Будесонид мите и Будесонид форте производится спейсер. Будесонид является составной частью комбинированного препарата Симбикорт.
Будесонид имеет наиболее благоприятный терапевтический индекс, что связано с его высоким сродством к глюкокортикоидным рецепторам, и ускоренным метаболизмом после системной абсорбции в легких и кишечнике. Будесонид является единственным ИГКС, для которого доказана возможность однократного применения. Фактор, обеспечивающий эффективность применения будесонида один раз в день, - ретенция будесонида в дыхательных путях в виде внутриклеточного депо благодаря обратимой эстерификации (образованию эфиров жирных кислот). При снижении концентрации свободного будесонида в клетке активируются внутриклеточные липазы, высвобождающийся из эфиров будесонид вновь связывается с рецептором. Подобный механизм не свойственен другим ГКС и позволяет пролонгировать противовоспалительный эффект. В ряде исследований показано, что внутриклеточное депонирование может оказаться более важным в плане активности препарата, чем сродство к рецептору.
Исследования последних лет по препарату Пульмикорт Турбухалер доказали, что он не влияет на конечный рост при длительном применении у детей, на минерализацию кости, не вызывает ангиопатию и катаракту. Пульмикорт также рекомендован к применению у беременных: установлено, что его применение не вызывает увеличения числа аномалий плода. Пульмикорт Турбухалер является первым и единственным ИГКС, которому FDA (организация по контролю за лекарственными средствами в США) присвоила категорию «В» в рейтинге лекарств, назначаемых при беременности. В эту категорию включаются лекарства, прием которых в период беременности является безопасным. Остальные ИГКС относятся к категории «С» (прием их во время беременности не рекомендуется).
Флютиказона пропионат . Самый высокоактивный препарат на сегодняшний день. Обладает минимальной пероральной биодоступностью (<1%). Эквивалентные терапевтические дозы флютиказона почти в два раза меньше, чем у беклометазона и будесонида в аэрозольном ингаляторе и сопоставимы с дозами будесонида в Турбухалере (табл. 2). По данным ряда исследований, флютиказона пропионат больше угнетает надпочечники, но в эквивалентных дозах имеет сходную с другими ИГКС активность в отношении надпочечников.
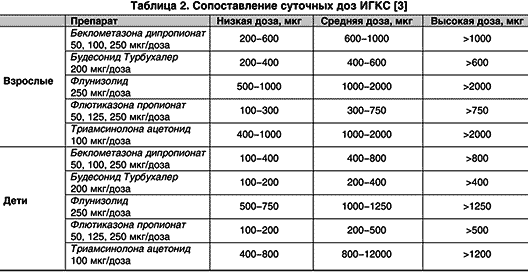
Представлен в виде дозированного аэрозольного ингалятора (Фликсотид 50, 125 и 250 мкг/доза) и порошкового ингалятора (Фликсотид Дискхалер - ротадиски 50, 100, 250 и 500 мкг/доза; Фликсотид Мультидиск 250 мкг/доза). Для аэрозольных ингаляторов производятся специальные спейсеры - «Волюматик» (клапанный спейсер большого объема для взрослых) и «Бэбихалер» (2-клапанный спейсер малого объема с силиконовой лицевой маской для детей раннего возраста). Флютиказон является составной частью комбинированного препарата Серетид Мультидиск.
Флунизолид . Препарат с низкой глюкокортикоидной активностью. На отечественном рынке представлен торговой маркой Ингакорт (дозированный ингалятор 250 мкг/доза, со спейсером). Несмотря на высокие терапевтические дозы, практически не имеет системных эффектов в связи с тем, что уже при первом прохождении через печень на 95% превращается в неактивное вещество. В настоящее время в клинической практике используется достаточно редко.
Триамсинолона ацетонид . Препарат с низкой гормональной активностью. Дозированный ингалятор 100 мкг/доза. Торговая марка Азмакорт, на российском рынке не представлен.
Мометазона фуроат . Препарат с высокой глюкокортикоидной активностью. На российском рынке представлен только в виде назального спрея Назонекс.
Клинические испытания, сравнивавшие эффективность ИГКС в виде улучшения симптомов и показателей функции внешнего дыхания, показывают, что:
- Будесонид и беклометазона дипропионат в аэрозольных ингаляторах при одинаковых дозах практически не отличаются по эффективности.
- Флютиказона пропионат обеспечивает такое же действие, как удвоенная доза беклометазона или будесонида в дозированном аэрозоле.
- Будесонид, применяемый через Турбухалер, оказывает такое же действие, как удвоенная доза будесонида в дозированном аэрозоле.
Нежелательные эффекты
Современные ИГКС относятся к препаратам с высоким терапевтическим индексом и имеют высокий профиль безопасности даже при длительном применении. Выделяют системные и местные нежелательные эффекты. Системные нежелательные эффекты могут стать клинически значимыми только при использовании высоких доз. Они зависят от сродства препаратов к рецептору, липофильности, объема распределения, периода полувыведения, биодоступности и других факторов. Риск возникновения системных нежелательных для всех имеющихся в настоящее время ИГКС коррелирует с желательными эффектами в дыхательных путях. Применение ИГКС в среднетерапевтических дозах снижает риск возникновения системных эффектов.
В основном побочные эффекты ИГКС связаны с их путем применения и сводятся к кандидозу полости рта, осиплости голоса, раздражению слизистой и кашлю. Чтобы избежать этих явлений, необходима правильная техника ингаляции и индивидуальный подбор ИГКС.
Комбинированные препараты
Несмотря на то, что ИГКС являются основой терапии БА, они не всегда позволяют полностью контролировать воспалительный процесс в бронхиальном дереве и, соответственно, проявления БА. В связи с этим возникала необходимость в назначении b 2 -агонистов короткого действия по потребности или регулярно. Таким образом появилась острая потребность в новом классе препаратов, свободных от недостатков, которые присущи b 2 -агонистам короткого действия, и обладающих доказанным длительным протективным и противовоспалительным действием на дыхательные пути.
Были созданы и в настоящее время широко применяются b 2 -агонисты длительного действия, которые на фармацевтическом рынке представлены двумя препаратами: формотерола фумаратом и сальметерола ксинафоатом. В современных руководствах по терапии астмы рекомендовано добавление b 2 -агонистов длительного действия при недостаточном контроле БА монотерапией ингаляционными ГКС (начиная со второй ступени). В ряде исследований было показано, что комбинация ингаляционного ГКС с b 2 -агонистом длительного действия более эффективна, чем удвоение дозы ингаляционных ГКС, и приводит к более значимому улучшению функции легких и лучшему контролю над симптомами астмы. Было показано также снижение количества обострений и значимое улучшение качества жизни у пациентов, получающих комбинированную терапию. Таким образом, появление комбинированных препаратов, содержащих ингаляционный ГКС и b 2 -агонист длительного действия, - отражение эволюции взглядов на терапию БА.
Главным преимуществом комбинированной терапии является повышение эффективности лечения при использовании более низких доз ИГКС. Кроме того, соединение двух препаратов в одном ингаляторе облегчает пациенту выполнение назначений врача и потенциально улучшает комплайнс.
Серетид Мультидиск . Составными компонентами являются сальметерола ксинафоат и флютиказона пропионат. Обеспечивает высокий уровень контроля над симптомами БА. Используется только в качестве базисной терапии, может назначаться, начиная со второй ступени. Препарат представлен в различных дозировках: 50/100, 50/250, 50/500 мкг сальметерола/флютиказона в 1 дозе. Мультидиск относится к ингаляционным устройствам малого сопротивления, что позволяет использовать его и у пациентов со сниженной скоростью вдоха.
Симбикорт Турбухалер . Составными компонентами являются будесонид и формотерола фумарат. На российском рынке представлен в дозировке 160/4,5 мкг в 1 дозе (дозы препаратов указаны как доза на выходе). Важная особенность Симбикорта - возможность использовать его как для базисной терапии (для контроля воспалительного процесса), так и для немедленного облегчения симптомов астмы. Это обусловлено прежде всего свойствами формотерола (быстрое начало действия) и способностью будесонида активно действовать в течение 24 часов на слизистую бронхиального дерева.
Симбикорт дает возможность индивидуального гибкого дозирования (1-4 ингаляционные дозы в сутки). Симбикорт можно использовать, начиная со 2 ступени, но особенно он показан пациентам с нестабильной астмой, для которой характерны внезапные тяжелые приступы затрудненного дыхания.
Системные ГКС
Системные ГКС применяются в основном для купирования обострения БА. Наиболее эффективны пероральные ГКС. Внутривенно кортикостероиды назначают при обострении БА, если более желателен внутривенный доступ, или при нарушении всасывания из желудочно-кишечного тракта, используя высокие дозы (до 1 г преднизолона, метилпреднизолона и гидрокортизона). Кортикостероиды приводят к клинически значимому улучшению спустя 4 часа после их введения.
При обострении БА показан короткий курс пероральных ГКС (7-14 дней), причем начинают с высоких доз (30-60 мг преднизолона). В последних публикациях рекомендуют следующий короткий курс системных ГКС при не угрожающих жизни обострениях: 6 таблеток преднизолона утром (30 мг) в течение 10 дней с последующим прекращением приема. Хотя схемы лечения системными ГКС могут быть различными, основополагающими принципами являются назначение их в высоких дозах для быстрого достижения эффекта и последующая быстрая отмена. Следует помнить, что как только пациент оказывается готовым к приему ингаляционных ГКС, они должны быть ему назначены с соблюдением ступенчатого подхода.
Системные глюкокортикоиды следует назначить, если:
- Обострение средней тяжести или тяжелое.
- Назначение ингаляционных b 2 -агонистов короткого действия в начале лечения к улучшению не привело.
- Обострение развилось, несмотря на то, что больной находился на длительном лечении пероральными кортикостероидами.
- Для купирования предыдущих обострений требовались пероральные кортикостероиды.
- 3 и более раз в год проводились курсы глюкокортикоидов.
- Больной находится на ИВЛ.
- Ранее были угрожающие жизни обострения.
Нежелательно использование пролонгированных форм системных стероидов для купирования обострений и проведения поддерживающей терапии БА.
Для длительной терапии при тяжелом течении БА системные ГКС (метилпреднизолон, преднизолон, триамсинолон, бетаметазон) следует назначать в наименьшей эффективной дозе. При длительном лечении альтернирующая схема назначения и прием в первой половине дня (для уменьшения влияния на циркадные ритмы секреции кортизола) вызывают наименьшее количество побочных эффектов. Следует подчеркнуть, что во всех случаях назначения системных стероидов больному должны быть назначены высокие дозы ингаляционных ГКС. Из пероральных ГКС предпочтение отдается тем, у которых отмечается минимальная минералокортикоидная активность, относительно короткий период полураспада и ограниченное действие на поперечно-полосатую мускулатуру (преднизолон, метилпреднизолон).
Стероидозависимость
Пациентам, которые вынуждены постоянно принимать системные ГКС, следует уделять особое внимание. Существует несколько вариантов формирования стероидозависимости у пациентов с БА и другими заболеваниями, сопровождающимися бронхообструкцией:
- Отсутствие комплайенса (взаимодействия) врача и пациента.
- Неназначение ингаляционных ГКС пациентам. Многие врачи считают, что нет необходимости назначать ингаляционные ГКС больным, получающим системные стероиды. Если пациент с БА получает системные стероиды, его следует расценивать, как больного с тяжелой формой БА, имеющего прямые показания к назначению высоких доз ингаляционных ГКС.
- У больных системными заболеваниями (включая легочные васкулиты, например, синдром Чардж-Стросса) бронхиальная обструкция может быть расценена, как БА. Отмена системных стероидов у этих больных может сопровождаться тяжелыми проявлениями системного заболевания.
- В 5% случаев встречается стероидорезистентность, для которой характерна резистентность стероидных рецепторов к стероидным препаратам. В настоящее время различают две подгруппы: больные с истинной стероидной резистентностью (тип II), не имеющие побочных эффектов при длительном приеме высоких доз системных ГКС, и пациенты с приобретенной резистентностью (тип I) - имеющие побочные эффекты системных ГКС. В последней подгруппе резистентность можно преодолеть, скорее всего, повышением дозы ГКС и назначением препаратов, имеющих аддитивный эффект.
1. Бронхиальная астма. Глобальная стратегия: совместный доклад Национального института Сердце, Легкие, Кровь и Всемирной организации здравоохранения. Пульмонология, 1996.
2. Бронхиальная астма. Руководство для врачей России (формулярная система). «Пульмонология», приложение-99.
3. Ведущие направления в диагностике и лечении бронхиальной астмы. Основные положения отчета группы экспертов EPR-2. National Institute of Health. National Heart, Lung and Blood Institute. NIH publication-97. Перевод под ред. Проф. Цой А.Н., М, Грантъ,1998.
4. Ильина Н.И. Ингаляционные глюкокортикоиды. Астма.ru. Аллергические и респираторные заболевания. 0*2001 (пилотный выпуск).
5. Огородова Л.М. Системы ингаляционной доставки препаратов в дыхательные пути. Пульмонология, 1999; №1, 84-87
6. Формулярная система: лечение бронхиальной астмы. Астма. ru ,0. 2001, 6-9
7. Чучалин А.Г. Бронхиальная астма. Москва, 1997.
8. Цой А.Н. Ингаляционные глюкокортикоиды: эффективность и безопасность. РМЖ 2001; 9: 182-185
9. Цой А.Н. Сравнительная фармакокинетика ингаляционных глюкокортикоидов. Аллергология 1999; 3: 25-33
10. Agertoft L., Pedersen S. Effect of long-term treatment with inhaled budesonide on adult height in children with asthma. N Engl J Med 2000; 343: 1064-9
11. Ankerst J., Persson G., Weibull E. A high dose of budesonide/formoterol in a single inhaler was well tolerated by asthmatic patients. Eur Respir J 2000; 16 (Suppl 31): 33s+poster
12. Barnes P.J. Inhaled glucocorticoides for asthma. N. Engl. Med. 1995; 332: 868-75
13. Beclomethasone Dipropionate and Budesonide. The clinical evidence Reviewed. Respir Med 1998; 92 (Suppl B)
14. The British Guidelines on Asthma Management. Thorax, 1997; 52 (Suppl. 1) 1-20.
15. Burney PGJ. Current questions in the epidemiology of asthma, in Holgate ST, et al, Asthma: Physiology. Immunology, and Treatment. London, Academic Press, 1993, pp 3-25.
16. Crisholm S et al. Once-daily budesonide in mild asthma. Respir Med 1998; 421-5
17. Kips JC, O/Connor BJ, Inman MD, Svensson K, Pauwels RA, O/Byrne PM. A long-termed study of the antiinflammatory effect of low-dosed budesonide plus formoterol versus high-dosed budesonide in asthma. Am Respir Crit Care Med 2000; 161: 996-1001
18. McFadden ER, Casale TB, Edwards TB et al. Administration of budesonide once daily by means of Turbuhaler to subjects with stable asthma. J Allergy Clin Immunol 1999; 104: 46-52
19. Miller-Larsson A., Mattsson H., Hjertberg E., Dahlback M., Tunek A., Brattsand R. Reversible fatty acid conjugation of budesonide: novel mechanism foe prolonged retention of topically applied steroid in airway tissue. Drug Metab Dispos 1998; 26: 623-30
20. Miller-Larsson A. et al. Prolonged airway activity and improved selectivity of budesonide possibly due to esterification. Am J Respir Crit Care Med 2000;162: 1455-1461
21. Pauwels RA et al. Effect of inhaled formoterol and budesonide on exacerbations of asthma. N Engl J Med 1997; 337: 1405-11
22. Pedersen S, O/Byrne P. A comparison of the efficacy and safety of inhaled corticosteroides in asthma. Allergy 1997; 52 (Suppl 39): 1-34.
23. Woolcock A.et al. Comparison of addition of salmeterol to inhaled steroids with doubling of the dose of inhaled steroids. Am J Respir Crit Care Med, 1996, 153, 1481-8.
Ингаляционные кортикостероиды рекомендуются с профилактической целью у больных с бронхиальной астмой персистирующего течения, начиная с легкой степени тяжести. Ингаляционные стероиды практически не имеют системных эффектов по сравнению с системными стероидами, однако высокие дозы ингаляционных стероидов следует с осторожностью использовать у больных, входящих в группу риска по развитию глаукомы и катаракты.
У меренные дозы ингаляционных кортикостероидов I и II поколения не вызывают супрессию коры надпочечников, а также не влияют на метаболизм костной ткани, однако при назначении их детям рекомендуется контролировать рост ребенка. Препараты III поколения можно назначать детям с возраста 1 год именно потому, что они обладают минимальным коэффициентом системной биодоступности. С целью достижения устойчивого эффекта ингаляционные формы кортикостероидов должны использоваться регулярно. Уменьшение симптомов астмы обычно достигается к 3-7-му дню терапии. При необходимости одновременного назначении |1г-агонистов и ингаляционных стероидов для лучшего проникновения последних в воздухоносные пути }
